Перейти к:
Формирование полибронхиального анастомоза при центральном раке легкого и буллезных изменениях с укрытием бронхиального шва свободным плеврально‑жировым лоскутом. Случай из клинической практики
https://doi.org/10.24060/2076-3093-2025-15-2-83-89
Аннотация
Введение. Бронхопластическая операция с формированием полибронхиального анастомоза при раке легкого позволяет избежать билобэктомии или пневмонэктомии. Цель — оценить результаты бронхопластической операции с формированием полибронхиального анастомоза при раке легкого. Материалы и методы. Минимальный стандартный объем хирургического лечения у нашего пациента — это нижняя билобэктомия справа, но с учетом буллезных изменений верхней доли правого легкого и остающихся трех сегментов этой же доли данное лечение привело бы к осложнениям после операции: разрыв буллы с формированием фистулы, инфицирование плевральной полости. Поэтому мы выполнили органосохранное лечение — средняя лобэктомия, сегментэктомия S6, циркулярная резекция промежуточного, нижнедолевого, сегментарного бронха B8 с формированием полибронхиального анастомоза между тремя бронхами. Для профилактики возникновения бронхоплеврального свища мы использовали свободный неваскуляризированный плеврально-жировой лоскут с перикардиальной области. Результаты. Послеоперационный период протекал без осложнений. Через 20 мес. после операции признаков рецидива не выявлено. Обсуждение. Бронхопластические операции дают возможность сохранить лучшее качество жизни по сравнению с пневмонэктомиями и билобэктомиями, при этом оставаясь радикальным методом лечения, без ухудшения показателей безрецидивной выживаемости. Заключение. Бронхопластические операции являются эффективным методом хирургического лечения рака легкого.
Ключевые слова
Для цитирования:
Гатьятов Р.Р., Зинченко С.В., Шаназаров Н.А. Формирование полибронхиального анастомоза при центральном раке легкого и буллезных изменениях с укрытием бронхиального шва свободным плеврально‑жировым лоскутом. Случай из клинической практики. Креативная хирургия и онкология. 2025;15(2):179-185. https://doi.org/10.24060/2076-3093-2025-15-2-83-89
For citation:
Gat’jatov R.R., Zinchenko S.V., Shanazarov N.A. Formation of Polybronchial Anastomosis in Central Lung Cancer with Bullous Changes Using Free Pericardial Fat Pad for Bronchial Suture Coverage: Clinical Case. Creative surgery and oncology. 2025;15(2):179-185. (In Russ.) https://doi.org/10.24060/2076-3093-2025-15-2-83-89
ВВЕДЕНИЕ
Проблема лечения злокачественных новообразований органов грудной клетки была и остается актуальной в силу того, что данная патология имеет широкое распространение и тенденцию к росту. В течение последних десятилетий рак легкого устойчиво занимает первое место в структуре заболеваемости и смертности от злокачественных новообразований [1]. Стандартизированный показатель заболеваемости раком легких в Челябинской области в 2021 году составил 25,3 на 100 000 жителей, в то время как в Российской Федерации он составлял 20,8 на 100 000 жителей [2].
Хирургическое лечение остается одним из основных методов терапии рака легкого наряду с химиотерапией и лучевой терапией. Основными операциями при раке легких являются анатомические резекции: лобэктомия и пневмонэктомия с систематической лимфодиссекцией [3]. Пневмонэктомия — это удаление целого легкого (правого или левого), поэтому данная операция переносится больными тяжело и сопровождается различными осложнениями в послеоперационном периоде и высокой летальностью (до 20 % по различным источникам) [4]. Бронхопластическая лобэктомия является альтернативой пневмонэктомии при центральном немелкоклеточном раке легкого [5][6]. В многочисленных публикациях представлены благоприятные результаты бронхопластических лобэктомий, которые характеризуются отдаленными результатами, сравнимыми с пневмонэктомией, и низкой послеоперационной смертностью [7–9]. Бронхопластические операции также связаны с лучшим качеством жизни по сравнению с пневмонэктомией за счет сохранения паренхимы легкого [10–12].
Для профилактики возникновения бронхоплеврального свища применяются различные васкуляризированные лоскуты [13]. В нашем клиническом примере мы использовали свободный неваскуляризированный плеврально-жировой лоскут с прекардиальной области.
Следует отметить, что трансплантация собственной жировой ткани в реконструктивной хирургии активно применяется уже более 20 лет, и жизнеспособность аутологичной жировой ткани основана на свойствах адипоцитов [14][15].
Цель исследования. В данной статье мы хотим поделиться результатом хирургического лечения больного центральным немелкоклеточным раком правого легкого с формированием полибронхиального анастомоза.
МАТЕРИАЛЫ И МЕТОДЫ
Больной К., 60 лет, находился в отделении торакальной онкологии ГАУЗ «Челябинский областной клинический центр онкологии и ядерной медицины» в апреле 2022 г. и болел центральным плоскоклеточным раком шестого сегментарного бронха нижней доли правого легкого (рис. 1).
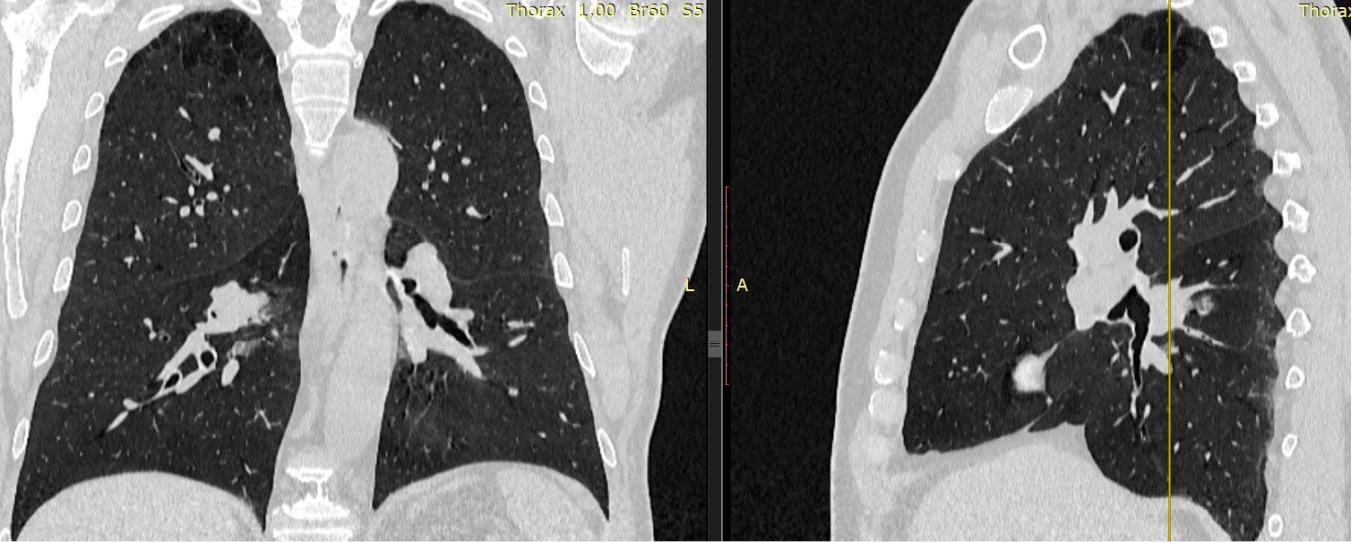
Рисунок 1. Центральный рак 6-го сегментарного бронха правого легкого
Figure 1. Central lung cancer of segmental bronchus B6 (Right)
В феврале 2022 г. после повышения температуры тела до 39 °C направлен по месту жительства на компьютерную томографию органов грудной клетки без контрастного исследования для исключения вирусной пневмонии. На этом исследовании выявлен центральный рак B6 нижней доли правого легкого. Пациенту в марте 2023 г. выполнена бронхоскопия: справа просвет 6-го сегментарного бронха в области устья обтурирован за счет инфильтративного новообразования бледно-розового цвета, выполнена биопсия опухоли, верифицирован умереннодифференцированный плоскоклеточный рак легкого. Выполнены обследования согласно клиническим стандартам: магнитно-резонансная томография головного мозга с контрастным усилением, компьютерная томография органов брюшной полости и забрюшинного пространства с контрастным усилением, остеосцинтиграфия костей скелета, ультразвуковое исследование шейных и надключичных лимфоузлов, оценена функция дыхания (в пределах нормальных значений). Признаков генерализации не выявлено. Проведен консилиум врачей: онколога, химиотерапевта и радиотерапевта — решено выполнить хирургическое лечение.
Минимальный стандартный объем хирургического лечения в данной ситуации — это нижняя билобэктомия справа с систематической лимфодиссекцией, но с учетом буллезных изменений верхней доли правого легкого (рис. 2) и остающихся трех сегментов из 10 данное лечение привело бы с большой долей вероятности к разрыву буллы с формированием фистулы, длительному сбросу воздуха, эмпиеме плевры.
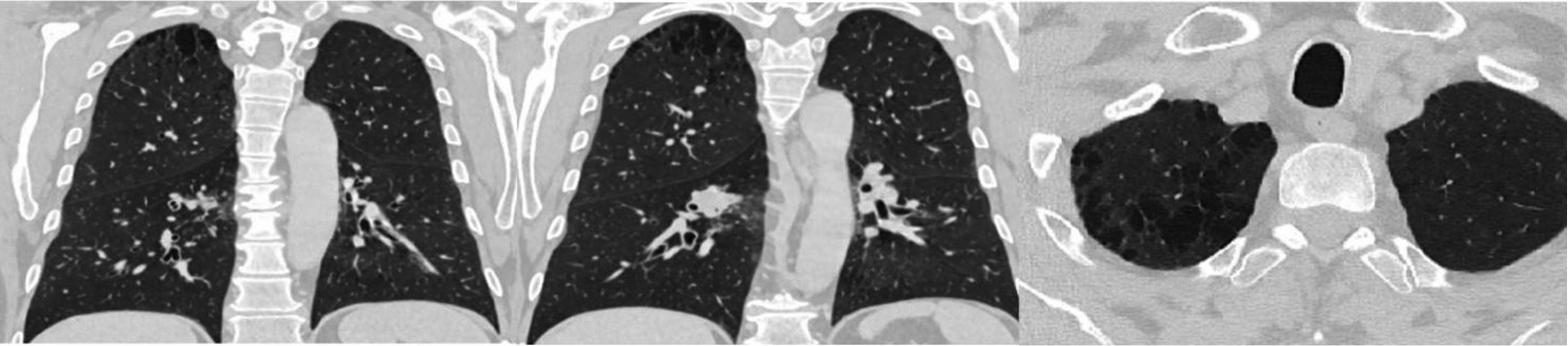
Рисунок 2. Буллезные изменения верхних долей легких на различных срезах при МСКТ органов грудной клетки
Figure 2. Bullous changes in upper lung lobes on axial chest MSCT slices
Поэтому мы выполнили органосохранное лечение — средняя лобэктомия, сегментэктомия S6, циркулярная резекция промежуточного, нижнедолевого, сегментарного бронха B8 с формированием полибронхиального анастомоза между тремя бронхами — схема и фото МСКТ сканов представлены на рисунках 3 и 4.
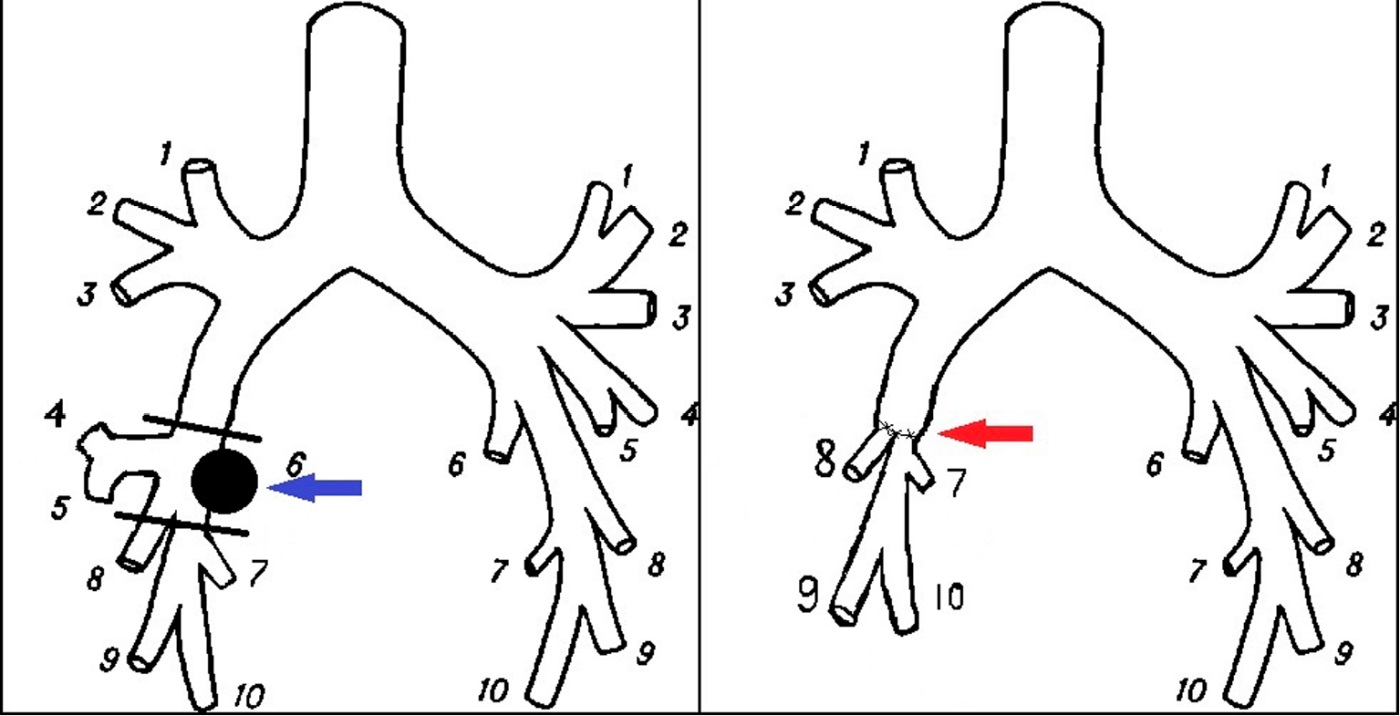
Рисунок 3. Схема объема резекции бронхов и сформированного полибронхиального анастомоза (на схеме: синяя стрелка — опухоль в В6, красная — анастомоз между бронхами)
Figure 3. Schematic of bronchial resection extent and polybronchial anastomosis formation (blue arrow — tumor in B6; red arrow — anastomosis between bronchi)
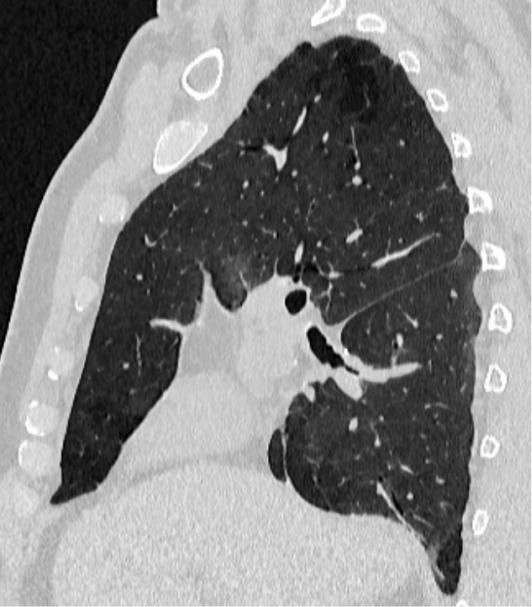
Рисунок 4. МСКТ-сканы объема резекции бронхов и сформированного полибронхиального анастомоза (желтым цветом указана резецируемая часть легкого и бронхов)
Figure 4. MSCT scans showing bronchial resection extent and polybronchial anastomosis formation (yellow highlights resected lung and bronchial tissue)
После резекции бронхов выполнили гистологический контроль всех краев резекции и, убедившись в отсутствии атипичных клеток по краям резекции, сформировали полибронхиальный анастомоз. Легочную артерию отвели с помощью турникета. На первом этапе узловыми швами нерассасывающейся нитью этибонд 3/0 сформировали новую карину бронха между 8-м сегментарным и нижнедолевым бронхом (рис. 5). На втором этапе узловыми швами рассасывающейся нитью викрил 3/0 сформирован циркулярный анастомоз между промежуточным и сегментарным B8 и нижнедолевым бронхом. Выполнен контроль герметичности бронхиальных швов, выявлено поступление воздуха в местах стыка трех бронхов, наложены П-образные швы, герметичность достигнута.
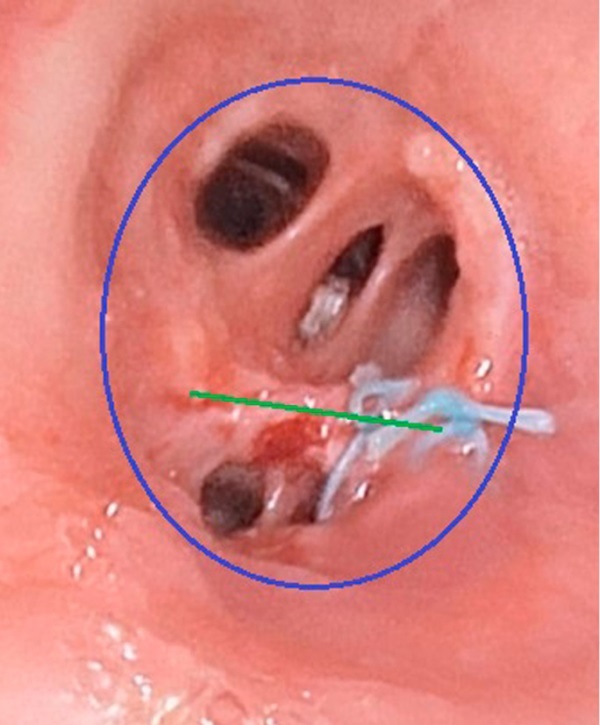
Рисунок 5. Полибронхиальный анастомоз через 4 мес. после операции — эндоскопическая картина
Figure 5. Endoscopic view of polybronchial anastomosis at four months postoperatively
На рисунке 5 представлена эндоскопическая картина через 4 месяца после операции. Здесь мы видим 2 узловых шва (этибонд 000 — нерассасывающейся материал) в области бронхиального шва между нижнедолевым бронхом и бронхом 8-го сегмента (новая картина бронхов — указана линией зеленого цвета). Циркулярный анастомоз между тремя бронхами (указан кругом синего цвета) без признаков стеноза и рецидива. Нити циркулярного анастомоза рассосались.
Выполнена систематическая лимфодиссекция: удалены лимфоузлы бифуркации трахеи, паратрахеальной группы, легочной связки, корня легкого.
Для дополнительного укрытия межбронхиального анастомоза из области перикарда переднего средостения сформирован свободный (без ножки) плеврально-жировой лоскут размерами 10×5×0,5 см. Данным лоскутом укрыт межбронхиальный анастомоз, лоскут фиксирован за края тремя узловыми швами викрил 3/0.
Длительность операции составила 280 минут. Кровопотеря 250 мл.
РЕЗУЛЬТАТЫ
Послеоперационный период протекал без осложнений. Удаление дренажей выполнено на четвертые сутки после операции. На 7-е сутки после хирургического лечения больной выписан.
Окончательное гистологическое заключение: плоскоклеточная неороговевающая карцинома ткани легкого, умеренной степени дифференцировки, образование размером 2,5×2,5×2,0 см. Края резекции — роста атипичных клеток не обнаружено. В удаленных лимфатических узлах кониофиброз, роста атипичных клеток не выявлено.
Окончательный клинический диагноз: центральный плоскоклеточный рак нижней доли правого легкого рT1cN0M0 R0G2 IA3 ст. С учетом радикального хирургического лечения и I стадии заболевания адъювантное лечение не назначено по решению консилиума врачей.
Через 25 мес. после операции пациент наблюдается у онколога по месту жительства без признаков рецидива и генерализации. На рисунке 6 представлены данные МСКТ грудной клетки и бронхоскопии.
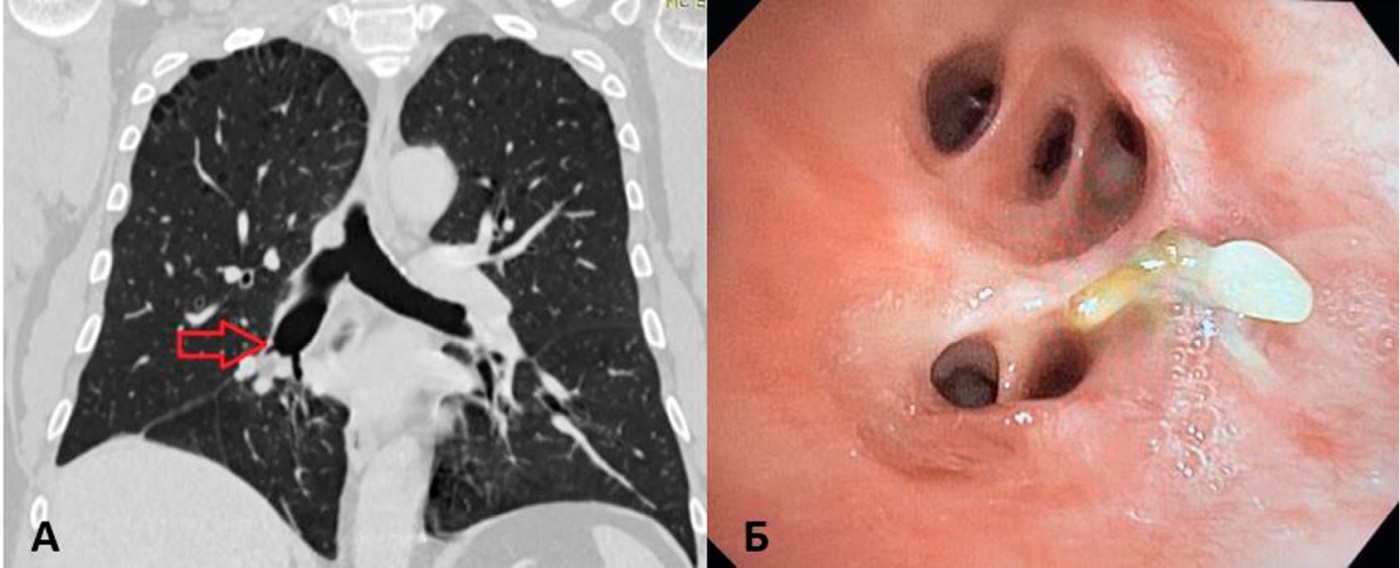
Рисунок 6. Рентгенологическая и эндоскопическая картина через 25 месяцев после операции. А — МСКТ органов грудной клетки с контрастным усилением (анастомоз указан красной стрелкой); Б — бронхоскопия через 25 месяцев после операции — признаков рецидива не выявлено
Figures 6. CT-scan and endoscopic picture 25 months after surgery. A — Contrast-enhanced chest MSCT (anastomosis marked by red arrow); Б — Bronchoscopy at 25 months postoperatively shows no signs of recurrence
ОБСУЖДЕНИЕ
Бурному развитию бронхопластической хирургии рака легкого способствовало стремление к органосохранным вмешательствам при центральных новообразованиях легкого. Реконструктивно-пластические операции при злокачественных новообразованиях применяют относительно редко, а операции с формированием полибронхиальных анастомозов еще реже, хотя многие авторы отмечают их высокую эффективность [3][16].
Бронхопластическая резекция легкого дает возможность сохранить полноценный хирургический контроль над первичной опухолью с гораздо меньшими последующими функциональными потерями. Целесообразность выполнения данного вида операции определяется в каждом отдельном случае индивидуально, стандартизованные подходы пока не разработаны [17].
Циркулярные бронхопластические операции в крупных лечебных центрах выполняются рутинно [4][18]. Но стоит указать, что рутинно выполняются рукавные (sleeve) бронхопластические лобэктомии (справа или слева) с анастомозом главного и промежуточного/нижнедолевого бронха, когда оба бронха лежат на одной линии/плоскости, распределение натяжения нити равномерное на протяжении всего бронхиального шва. При выполнении бронхопластической операции с формированием полибронхиального анастомоза необходимо создать анастомоз между тремя бронхами, очень сложно добиться герметичности данного анастомоза, поэтому риски возникновения бронхоплеврального свища возрастают. Именно поэтому подобные операции выполняются редко и поэтому необходимо дополнительное укрытие межбронхиального шва пластическим материалом для профилактики возникновения бронхо-плеврального свища [19].
Чтобы минимизировать риск несостоятельности бронхиальных швов, хирурги предложили новую стратегию — дополнительное интраоперационное укрытие швов бронха. Для этого применяют различные пластические материалы, способные улучшить кровоснабжение тканей в зоне шва: мышечные лоскуты, париетальную плевру, диафрагмальный лоскут, непарную вену, перикардиальный лоскут и тимус. Особое значение укрытие бронхиальных швов приобретает при выполнении комбинированных резекций и в ситуации, когда перед операцией проводилось предоперационное лечение [20].
Несмотря на разнообразие существующих методик, специалисты не пришли к единому мнению о способах профилактики несостоятельности швов культи бронха. При этом данные, полученные в ходе исследований, имеют ограниченное применение при решении вопроса о дополнительном укрытии межбронхиальных анастомозов. В частности, использование мышечных лоскутов для укрытия межбронхиальных анастомозов сопряжено с риском стеноза в области анастомоза или тромбозом питающего лоскут сосуда и его некрозом, что ограничивает возможность применения данного метода [21].
При выборе лоскута для укрытия бронхиального шва необходимо соблюдать определённые параметры: лоскут должен быть достаточно длинным, но при этом иметь небольшую ширину. Однако такая конфигурация создает риск нарушения кровоснабжения в дистальных участках трансплантата. Поэтому в данном клиническом случае мы использовали свободный перикардиальный плеврально-жировой лоскут. Данный лоскут выкраивается из париетальной плевры с жировой клетчаткой в области перикарда переднего средостения. Технически данный стебель формируется без особых трудностей и требует затраты не более 15 минут.
Данным свободным лоскутом можно укрыть как бронхиальные швы культи бронха, так и швы межбронхиальных анастомозов после различных бронхопластических операций. Свободный лоскут дает возможность перемещать его в любое место, которое необходимо дополнительно укрыть, а лоскуты на ножке ограничены в перемещении.
ЗАКЛЮЧЕНИЕ
Таким образом, бронхопластические операции дают возможность сохранить больному больше паренхимы легкого и улучшить качество жизни по сравнению с пневмонэктомиями и билобэктомиями, при этом оставаясь радикальным методом лечения рака легкого, без значительного ухудшения показателей безрецидивной выживаемости.
Список литературы
1. Каприн А.Д., Старинский В.В., Шахзадова А.О. (ред.) Злокачественные новообразования в России в 2021 году (заболеваемость и смертность). М.: МНИОИ им. П.А. Герцена — филиал ФГБУ «НМИЦ радиологии» Минздрава России; 2021.
2. Мерабишвили В.М., Юркова Ю.П., Щербаков А.М., Левченко Е.В., Барчук А.А., Кротов Н.Ф. и др. Рак легкого (С33, 34). Заболеваемость, смертность, достоверность учета, локализационная и гистологическая структура (популяционное исследование). Вопросы онкологии. 2021;67(3):361–7. DOI: 10.37469/0507-3758-2021-67-3-361-367
3. Левченко Е.В., Шабинская В.И., Левченко Н.Е., Михнин А.Е., Мамонтов О.Ю., Ергнян С.М. и др. Сравнение результатов лечения НМРЛ после бронхопластических резекций и пневмонэктомий. Вопросы онкологии. 2024;70(2):316–23. DOI: 10.37469/0507-3758-2024-70-2-316-323
4. Пикин О.В., Рябов А.Б., Глушко В.А., Колбанов К.И., Багров В.А., Александров О.А. и др. Реконструктивная резекция легкого в рутинной клинической практике: опыт одного центра. Грудная и сердечно-сосудистая хирургия. 2022;64(5):524–32. DOI: 10.24022/0236-2791-2022-64-5-524-532
5. Топольницкий Е.Б., Шефер Н.А. Непосредственные результаты ангио- и бронхопластических лобэктомий при немелкоклеточном раке легкого у пациентов старше 70 лет. Хирургия. Журнал им. Н.И. Пирогова. 2022;6:48–54. DOI: 10.17116/hirurgia202206148
6. Аксарин А.А., Тер-Ованесов М.Д., Копейка С.М. Бронхопластические операции в лечении больных немелкоклеточным раком легкого. Сибирский онкологический журнал. 2022;21(1):85–90. DOI: 10.21294/1814-4861-2022-21-1-85-90
7. Пилькевич Д.Н., Довбня С.А., Хольный М.П., Цвиренко А.С. Опыт применения трахео-бронхопластических операций при раке легкого. Уральский медицинский журнал. 2021;20(4):46–52. DOI: 10.52420/2071-5943-2021- 20-4-46-52
8. Харагезов Д.А., Мирзоян Э.А., Козель Ю.Ю., Мкртчян Г.А., Антонян А.А., Айрапетова Т.Г. и др. Случай выполнения бронхопластической операции пациентке пятнадцати лет с редкой аденокистозной карциномой легкого. Южно-Российский онкологический журнал. 2024;5(4):38–45. DOI: 10.37748/2686-9039-2024-5-4-5
9. Каменев Р.О., Руденко М.С., Елисеева А.П., Глазков Г.К. Бронхопластические операции по поводу опухолей легкого различной этиологии. Собственный опыт. Уральский медицинский журнал. 2024;23(4):138–47. DOI: 10.52420/umj.23.4.138
10. Атюков М.А., Земцова И.Ю., Петров А.С., Жемчугова-Зеленова О.А., Новикова О.В., Мищеряков С.А. и др. Ближайшие результаты бронхопластических лобэктомий, выполненных из видеоторакоскопического и торакотомного доступов. Вестник хирургии им. И. И. Грекова. 2022;181(4):20–8. DOI: 10.24884/0042-4625-2022-181-4-20-28
11. Шефер Н.А., Топольницкий Е.Б. Методологические аспекты ангио- и бронхопластических лобэктомий при раке легкого у больных пожилого и старческого возраста. Вопросы реконструктивной и пластической хирургии. 2023;26(2):25–34. DOI: 10.52581/1814-1471/85/03
12. Hishida T., Aokage K., Yoshida J., Miyoshi T., Tsuboi M. Extended bronchoplasty for locally advanced left lower lobe lung cancer: surgical technique and outcomes. Interact Cardiovasc Thorac Surg. 2018;27(4):602–5. DOI: 10.1093/icvts/ivy081
13. Баксиян Г.А., Завьялов А.А. Бронхиальный свищ — грозное и коварное осложнение в онкологической практике. Клинический вестник ФМБЦ им А.И. Бурназяна. 2023;3:41–6. DOI: 10.33266/2782-6430-2023-3-41-46
14. Пахомова Р.А., Клименко К.В. Исторические аспекты и перспективы развития пересадки аутологичной жировой ткани (обзор литературы). Московский хирургический журнал. 2023;4:81–7. DOI: 10.17238/2072-3180-2023-4-81-87
15. Храмцова Н.И., Плаксин С.А., Соцков А.Ю., Пономарев Д.Н. Применение методики аутотрансплантации жировой ткани у пациентов с контурными деформациями, дефектами кожи и мягких тканей. Пермский медицинский журнал. 2022;39(4):97–107. DOI: 10.17816/pmj39497%107
16. Marshall M.B., Sugarbaker E.A. Bronchoplasty for pulmonary preservation: A novel technique. JTCVS Tech. 2023;19:132–4. DOI: 10.1016/j.xjtc.2023.03.010
17. Girelli L., Bertolaccini L., Casiraghi M., Petrella F., Galetta D., Mazzella A., et al. Anastomosis complications after bronchoplasty: incidence, risk factors, and treatment options reported by a referral cancer center. Curr Oncol. 2023;30(12):10437–49. DOI: 10.3390/curroncol30120760
18. Qi K., Lin G., Liu H., Zhang X., Huang W., Chen Z., et al. Safety and feasibility of preferential manual bronchoplasty in 2-3 cm single-port video-assisted thoracoscopic lobectomy. Thorac Cancer. 2023;14(24):2484–92. DOI: 10.1111/1759-7714.15033
19. Peng Z., Mei J., Liu C., Guo C., Gonzalez M., Bölükbas S., et al. Risk factors and outcomes of bronchopleural fistula after bronchoplasty in patients with non-small cell lung cancer: a retrospective multivariate analysis. Transl Lung Cancer Res. 2022;11(5):744–56. DOI: 10.21037/tlcr-22-272
20. Никулин А.В., Романихин А.И., Гандыбина Е.Г., Петровская А.А., Паталова А.Р., Абдуллах Я. и др. Вопросы закрытия бронхоплеврального свища на фоне эмпиемы плевры. Хирургическая практика. 2024;4:42–58. DOI: 10.5922/2223-2427-2024-9-4-4
21. Корымасов Е.А., Медведчиков-Ардия М.А., Поляков И.С., Бенян А.С. Этапная реконструктивно-восстановительная хирургия при бронхоплевральном свище. Хирургия. Журнал им. Н.И. Пирогова. 2023;4:61–5. DOI: 10.17116/hirurgia202304161
Об авторах
Р. Р. ГатьятовРоссия
Гатьятов Рудольф Рашитович — отделение торакальной онкологии
Челябинск
С. В. Зинченко
Россия
Зинченко Сергей Викторович — д.м.н., доцент, кафедра хирургии
Республика Татарстан, Казань
Н. А. Шаназаров
Казахстан
Шаназаров Насрулла Абдуллаевич — д.м.н., профессор
Астана
Рецензия
Для цитирования:
Гатьятов Р.Р., Зинченко С.В., Шаназаров Н.А. Формирование полибронхиального анастомоза при центральном раке легкого и буллезных изменениях с укрытием бронхиального шва свободным плеврально‑жировым лоскутом. Случай из клинической практики. Креативная хирургия и онкология. 2025;15(2):179-185. https://doi.org/10.24060/2076-3093-2025-15-2-83-89
For citation:
Gat’jatov R.R., Zinchenko S.V., Shanazarov N.A. Formation of Polybronchial Anastomosis in Central Lung Cancer with Bullous Changes Using Free Pericardial Fat Pad for Bronchial Suture Coverage: Clinical Case. Creative surgery and oncology. 2025;15(2):179-185. (In Russ.) https://doi.org/10.24060/2076-3093-2025-15-2-83-89


































