Перейти к:
Спиртовая септальная абляция при гипертрофической кардиомиопатии с обструкцией выходного тракта левого желудочка под контролем контрастной эхокардиографии
https://doi.org/10.24060/2076-3093-2019-9-2-132-137
Аннотация
В ГБУЗ «Республиканский кардиологический центр» в 2015 г. внедрена методика спиртовой септальной абляции. В статье представлен один из случаев успешного лечения пациента с гипертрофической кардиомиопатией с обструкцией выходного тракта левого желудочка с помощью методики алкогольной септальной абляции с применением ультразвукового эхокардиографического контроля зоны повреждения межжелудочковой перегородки.
Ключевые слова
Для цитирования:
Николаева И.Е., Плечев В.В., Мухаметьянов А.М., Бикташев Р.М., Бузаев И.В., Халикова Г.А. Спиртовая септальная абляция при гипертрофической кардиомиопатии с обструкцией выходного тракта левого желудочка под контролем контрастной эхокардиографии. Креативная хирургия и онкология. 2019;9(2):132-137. https://doi.org/10.24060/2076-3093-2019-9-2-132-137
For citation:
Nikolaeva I.E., Plechev V.V., Mukhametyanov A.M., Biktashev R.M., Buzaev I.V., Khalikova G.A. Contrast Enhanced Echocardiography-Controlled Alcohol Septal Ablation for Hypertrophic Cardiomyopathy with Left Ventricular Outflow Tract Obstruction. Creative surgery and oncology. 2019;9(2):132-137. (In Russ.) https://doi.org/10.24060/2076-3093-2019-9-2-132-137
Введение
Гипертрофическая кардиомиопатия (ГКМП) — генетическая патология, выражающаяся структурной и функциональной аномалией миокарда левого желудочка, проявляющаяся утолщением стенок по данным ЭхоКГ, КТ или МРТ. У части пациентов гипертрофия миокарда может приводить к обструкции выходного тракта левого желудочка (ВТЛЖ), что обуславливает высокий риск неблагоприятных сердечно-сосудистых исходов. Критерием обструкции ВТЛЖ является максимальный градиент давления (ГДmax) в ВТЛЖ > 25 мм рт. ст. по данным ЭхоКГ. При ГДmax > 50 мм рт. ст. рассматривается вопрос о выполнении коррекции ВТЛЖ [1-3]. Показания к коррекции ВТЛЖ определяются высокими цифрами градиента давления, недостаточностью кровообращения 3-4-го функционального класса по NYHA, наличием синкопальных состояний и неэффективностью медикаментозной терапии [1].
В настоящее время устранение субаортальной обструкции выполняется двумя способами: миоэктомии на открытом сердце и эндоваскулярным способом. В нашей статье мы хотели описать вариант лечения обструктивной формы ГКМП с помощью транскатетерного метода [4].
Впервые септальная абляция у больных с обструктивной формой ГКМП была осуществлена в 1994 г. F. Gietzen и его коллегами [5]. Они использовали технику чрескожной транслюминальной ангиопластики с последующим введением 96 % этанола в перфорантную септальную ветвь, что приводило к локализованному инфаркту и уменьшению толщины МЖП с последующим снижением субаортальной обструкции.

Рисунок 1. Передняя межжелудочковая артерия отдает множественные мелкие септальные ветви. Случай, не подходящий для септальной абляции
Figure 1. Anterior interventricular artery with multiple small septal branches. Septal ablation contraindicated
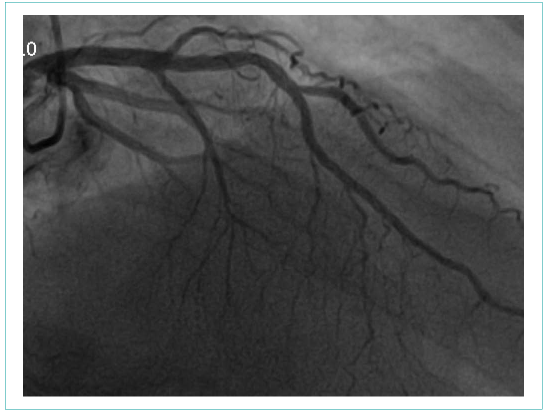
Рисунок 2. Передняя межжелудочковая артерия отдает крупную септальную ветвь
Figure 2. Anterior interventricular artery with a large septal branch
Сегодня во всем мире операция спиртовой септальной абляции выполняется в немногих медицинских центрах, включая ГБУЗ «Республиканский кардиологический центр».
Техническая возможность выполнения септальной абляции определяется наличием перфорантных внутриперегородочных ветвей более 1 мм и отсутствием их участия в кровоснабжении папиллярных мышц. Оценка строения септальных ветвей выполняется при коронарографии.
В связи с тем что расположение септальных артерий в миокарде индивидуально, информация об участке миокарда, который нужно разрушить инъекцией спирта, крайне необходима перед выполнением абляции, чтобы исключить повреждение гемодинамически значимых структур миокарда, таких как папиллярные мышцы.
Оценка зоны кровоснабжения септальной ветви выполняется методом селективной контрастной трансторакальной эхокардиографии. Выполняется следующими образом: в септальную ветвь в приустьевом отделе over the wire (OTW) баллонным катетером через просвет OTW-баллонного катетера вводится ультразвуковое контрастное средство, распределяющееся в зоне кровоснабжения септальной ветви. В течение времени, необходимого для выполнения эхокардиографического определения зоны распределения контрастного вещества, баллонный катетер должен оставаться достаточно раздутым, препятствуя смыванию ультразвукового контраста (рис. 3) [6, 7].
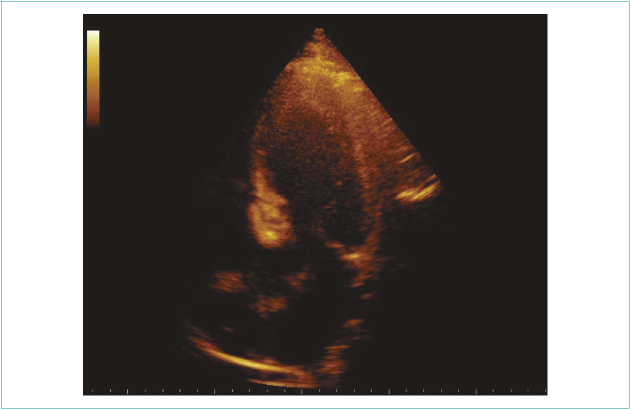
Рисунок 3. Определяется контрастное вещество в пределах базального сегмента межжелудочковой перегородки
Figure 3. Contrast agent in basal segment of interventricular septum
Материалы и методы
Собственный клинический случай
Пациентка В., 50 лет, с 2008 г. наблюдалась с диагнозом «гипертрофическая кардиомиопатия». С ноября 2018 г. отмечала ухудшение самочувствия в виде выраженной одышки, давящих болей за грудиной, преимущественно при физической нагрузке (при ходьбе до 100 м и подъеме на 2-й этаж), неоднократных эпизодах синкопальных состояний. По данным ЭхоКГ обращали внимание следующие показатели: толщина межжелудочковой перегородки 1,7-1,9 см, градиент давления на выходном тракте ЛЖ 130 мм рт. ст. в покое, систолическое давление в правом желудочке (СДПЖ) 90 мм рт. ст., умеренная митральная недостаточность, незначительное количество выпота в полости перикарда, фракция выброса составляла 67 % Sim. Принимаемое лечение — метопролол сукцинат 100 мг утром, периндоприл 2,5 мг вечером, кардиомагнил 150 мг. Назначить более высокие дозы метопролола не позволяло низкое артериальное давление.
Также в анамнезе у пациентки отмечалась диагностированная кавернозная ангиома головного мозга. Состояние при поступлении средней тяжести. Сознание ясное. Кожные покровы физиологической окраски. Дыхание жесткое, хрипов нет. ЧД 17 в минуту. Сердечные тоны усилены, расщепление 2 тона и систолический шум на аортальном клапане типа crescendo-decrescendo. Пульс 65 ударов в минуту. АД 120/90 мм рт. ст. Отечность нижних конечностей до середины голеней.
Учитывая высокую степень субаортальной обструкции, клиническое состояние пациентки, отсутствие эффективности медикаментозной терапии и наличие высокого риска осложнений при открытой миоэктомии, было решено провести спиртовую септальную абляцию.
На коронарографии определись интактные коронарные артерии, выраженная первая септальная ветвь (СВ1) передней межжелудочковой артерии (ПМЖА), мышечный мост в среднем сегменте ПМЖА с систолической компрессией до 40 % (видео 1).
Видео 1. Селективное контрастирование левой коронарной артерии
Video 1. Selective contrast enhancement of left coronary artery
Правая коронарная артерия была интактна (видео 2).
Видео 2. Селективное контрастирование правой коронарной артерии
Video 2. Selective contrast enhancement of right coronary artery
Премедикация в операционной — диазепам 10 мг, промедол 20 мг.
Ход операции. Электрод временного электрокардиостимулятора (ЭКС) установлен в правый желудочек, контроль положения электрода пробным навязыванием ритма. Инвазивное измерение градиента давления в ВТЛЖ, ГД в покое 105 мм рт. ст., при пробе Вальсальвы 125 мм рт. ст.
Устье ЛКА канюлировано проводниковым катетером. По коронарному проводнику в септальную ветвь проведен OTW-баллонный катетер, проводник удален (видео 3). Раздутием баллона окклюзирована септальная ветвь, в септальную ветвь введено ультразвуковое контрастное вещество серы гексафторид (соновью) 2,0 мл (видео 4). На ЭхоКГ контрастное вещество распределилось в пределах базального сегмента межжелудочковой перегородки (видео 5 и 6). После чего в септальную ветвь введено 2,0 мл 96 % раствора этилового спирта с экспозицией 20 минут (видео 7 и 8). Баллон сдут и удален. На контрольной коронарографии первая септальная ветвь не контрастируется, контрастирование передней межжелудочковой артерии не изменено (видео 9). Интраоперационно по данным ЭхоКГ ГД в ВТЛЖ снизился до 53-60 мм рт. ст.
Видео 3. В первую септальную ветвь проведен коронарный проводник
Video 3. Coronary guidewire in first septal branch
Видео 4. Баллонный катетер раздут в первой септальной ветви
Video 4. Balloon catheter inflated in first septal branch
Видео 5. Контрастная эхокардиография в апикальной четырехкамерной позиции
Video 5. Contrast enhanced echocardiography, apical four-chamber view
Видео 6. Контрастная эхокардиография в апикальной двухкамерной позиции
Video 6. Contrast enhanced echocardiography, apical two-chamber view
Видео 7. Введение 96 % спирта с добавлением контраста
Video 7. Injection of 96% alcohol with added contrast agent
Видео 8. 10-минутная экспозиция 96 % спирта
Video 8. 10 minutes exposure to 96% alcohol
Видео 9. Контрольная коронарография
Video 9. Control coronary angiography. No contrast visualisation of first septal branch
В раннем послеоперационном периоде суточное наблюдение в условиях отделения реанимации и интенсивной терапии (ОРИТ). Двукратное срабатывание ЭКС. Тропониновый тест положительный. Электрод ЭКС удален на 2-е сутки.
На 3-е сутки по данным ЭхоКГ отмечалась локальная редукция толщины базальной части МЖП до 1,3 см с гипокинезом на небольшом участке с сохранением общей сократительной способности левого желудочка (ФВ 60 % Sim), ГД на выходном тракте ЛЖ составлял 65 мм рт. ст., наблюдалось уменьшение степени регургитации на митральном клапане и снижение СДПЖ до 45 мм рт. ст.
Через 2 мес. при проведении контрольной ЭхоКГ было зафиксировано увеличение ГД до 85 мм рт. ст. У пациентки, несмотря на улучшение самочувствия (повысилась толерантность к физической нагрузке, уменьшились отеки на ногах, перестали беспокоить кардиальные боли) и принимаемую медикаментозную терапию (в т. ч. максимальные для нее дозы β-блокаторов), сохранялась выраженная одышка.
Учитывая высокую степень обструкции на выходном тракте ЛЖ, жалобы пациентки на одышку, оптимальное строение и расположение второй ветви, было решено провести повторную абляцию.
После абляции второй септальной ветви интраоперационно ГД в ВТЛЖ составил 43 мм рт. ст.
На контрольной ЭхоКГ через 3 суток отмечалась гипертрофия базального сегмента МЖП до 1,2 см с локальным истончением на небольшом протяжении до 0,8 см с уменьшением контрактильной способности на этом участке и сохранением общей сократительной способности левого желудочка (ФВ 62 % Sim), ГД в выходном тракте ЛЖ 20-22 мм рт. ст., СДПЖ 35 мм рт. ст. (рис. 4). Данные показатели сохранялись при проведении контрольной ЭхоКГ через 1, 3, 6 мес.
Клинически у больной отмечалось улучшение самочувствия, в том числе значительное уменьшение одышки.
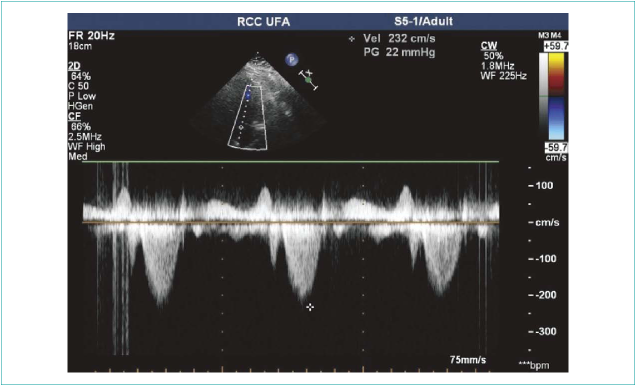
Рисунок 4. Доплерограмма выходного тракта левого желудочка после септальной абляции
Figure 4. Left ventricular outflow tract Doppler post septal ablation
Обсуждение
По данным литературы, устранение или значительное снижение градиента давления в выходном тракте левого желудочка наблюдается более чем у 90 % больных ГКМП после хирургического вмешательства, что приводит к значительному улучшению клинической картины в 70-80 % случаев [8, 9]. Несмотря на большой опыт лечения этого заболевания, остается высокая летальность у пациентов с ХСН 3-4 ФК (42 %) [10]. В нашем случае, несмотря на проводимую адекватную медикаментозную терапию с высокими дозами β-блокаторов, у пациентки наблюдалась клиническая картина выраженной сердечной недостаточности и сохранялись высокие значения градиента давления в выходном тракте ЛЖ. Ситуацию усугубляло наличие установленной кавернозной ангиомы головного мозга. После продолжительного обсуждения, учитывая высокий риск осложнений при открытой миоэктомии, было решено провести септальную миоабляцию. Хирургическая коррекция была эффективной, несмотря на двукратное вмешательство. Повышение субаортального ГД после первой операции, видимо, было связано с редукцией базальной части МЖП на недостаточном протяжении и ремоделированием миокарда.
После второй абляции были достигнуты оптимальные значения градиента давления, которые сохранялись в течение 6 месяцев, и улучшение других показателей по данным ЭхоКГ. Также хотелось отметить, что, несмотря на индуцированный локализованный инфаркт, общая сократительная способность миокарда не пострадала. Одновременно с положительным изменением показателей данных инструментальных обследований отмечалось выраженное улучшение самочувствия больной и компенсация хронической сердечной недостаточности.
Заключение
Спиртовая септальная абляция является малоинвазивным, эффективным и относительно безопасным методом лечения гипертрофической обструктивной кардиомиопатии при резистентности к медикаментозной терапии. Также может быть лечением выбора при наличии высокого риска осложнений операции на открытом сердце. А выполнение контрастной эхо-кардиографии позволяет диагностировать зоны, допустимые для введения этанола, исключить повреждение гемодинамически значимых структур миокарда и этим самым повысить безопасность хирургического лечения.
Список литературы
1. ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy. Eur Heart J. 2014;35(39):2733–79. DOI: 10.1093/eurheartj/ ehu284
2. Mischi M. Contrast echocardiography for cardiac quantifications [dissertation]. Eindhoven: Technische Universiteit Eindhoven; 2004. DOI: 10.6100/IR579395
3. Бокерия Л.А. Гипертрофическая обструктивная кардиомиопатия. Анналы хирургии. 2013;(5):5–14.
4. Каплунова В.Ю., Шакарьянц Г.А., Кожевникова М.В., Хабарова Н.В., Привалова Е.В., Беленков Ю.Н. Современные подходы к проблеме гипертрофической кардиомиопатии. Клиническая медицина. 2016;94(10):754–63. DOI: 10.18821/0023-2149-2016-94- 10-754-763
5. Gietzen F., Leuner C., Gerenkapm T., Kuhn H. Relief of obstruction in hypertrophic cardiomyopathy by transient occlusion of the first septal branch of the left coronary artery. Eur Heart J. 1994;15(Suppl.):125. DOI: 10.1093/eurheartj/15.Abstract_Supplement.1
6. Mukherjee D., Bates E.R., Roffi M., Lange R.A., Moliterno D.J. Cardiovascular catheterization and intervention: a textbook of coronary, peripheral, and structural heart disease. 2nd ed. Boca Raton: CRC Press; 2018.
7. Осиев А.Г., Гегенава Б.Б., Палеев Ф.Н., Григорьева Н.М. Спиртовая септальная аблация межжелудочковой перегородки с контрастным эхокардиографическим контролем. Российский кардиологический журнал. 2017;22(8):122–7. DOI: 10.15829/1560-4071-2017- 8-122-127
8. Осиев А.Г., Кретов Е.И., Курбатов В.П., Мироненко С.П., Найденов Р.А., Артамонова Е.А. и др. Новый подход к оценке результатов транскоронарной септальной аблации у больных с гипертрофической обструктивной кардиомиопатией. Патология кровообращения и кардиохирургия. 2013;17(3):46–9. DOI: 10.21688/1681-3472-2013-3-46-49
9. Maron B.J., Tpstein S.E., Morrow A.G. Symptomatic status and prognosis of patients after operation for hypertrophic obstructive cardiomyopathy: efficacy of ventricular septal myotomy and myectomy. Eur Heart J. 1983;4(Suppl. F):175–85. DOI: 10,1093 / eurheartj / 4.suppl_f.175
10. Schulte H.D., Gramsch-Zabel H., Schwartzkopff R. Hypertrophic obstructive cardiomyopathy: surgical management. Schweiz Med Wochenschr. 1995;125(41):1940–9. PMID: 7481652
Об авторах
И. Е. НиколаеваРоссия
Николаева Ирина Евгеньевна — к.м.н., главный врач, главный внештатный кардиолог Министерства здравоохранения Республики Башкортостан
В. В. Плечев
Россия
Плечев Владимир Вячеславович — д.м.н., профессор, член-корр. АН РБ, зав. кафедрой госпитальной хирургии, член президиума общественной организации «Ассоциация хирургов Республики Башкортостан»
А. М. Мухаметьянов
Россия
Мухаметьянов Азат Минисламович — врач по рентгенэндоваскулярным диагностике и лечению
Р. М. Бикташев
Россия
Бикташев Ренат Марисович — врач по рентгенэндоваскулярным диагностике и лечению
И. В. Бузаев
Россия
Бузаев Игорь Вячеславович — к.м.н., зав. отделением рентген-хирургических методов диагностики и лечения № 1, доцент кафедры госпитальной хирургии
Г. А. Халикова
Россия
Халикова Гульчачак Амировна — к.м.н., врач функциональной диагностики
Дополнительные файлы

|
1. 1. Селективное контрастирование левой коронарной артерии. Определяется хорошо выраженная первая септальная ветвь и мышечный мост в среднем сегменте ПМЖА | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(7MB)
|
Метаданные ▾ | |

|
2. 2. Селективное контрастирование правой коронарной артерии. Контуры артерий четкие, ровные на всем протяжении | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(7MB)
|
Метаданные ▾ | |

|
3. 3. В первую септальную ветвь проведен коронарный проводник | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(4MB)
|
Метаданные ▾ | |

|
4. 4. Баллонный катетер раздут в первой септальной ветви | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(9MB)
|
Метаданные ▾ | |

|
5. 5. Контрастная эхокардиография в апикальной четырехкамерной позиции. Визуализируется ультразвуковой контраст в пределах базального сегмента межжелудочковой перегородки | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(24MB)
|
Метаданные ▾ | |

|
6. 6. Контрастная эхокардиография в апикальной двухкамерной позиции. Визуализируется ультразвуковой контраст в пределах базального сегмента межжелудочковой перегородки | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(29MB)
|
Метаданные ▾ | |

|
7. 7. Введение 96% спирта с добавлением контраста | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(16MB)
|
Метаданные ▾ | |

|
8. 8. 10-минутная экспозиция 96% спирта | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(11MB)
|
Метаданные ▾ | |

|
9. 9. Контрольная коронарография. Контрастирование первой септальной ветви не определяется | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(10MB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Николаева И.Е., Плечев В.В., Мухаметьянов А.М., Бикташев Р.М., Бузаев И.В., Халикова Г.А. Спиртовая септальная абляция при гипертрофической кардиомиопатии с обструкцией выходного тракта левого желудочка под контролем контрастной эхокардиографии. Креативная хирургия и онкология. 2019;9(2):132-137. https://doi.org/10.24060/2076-3093-2019-9-2-132-137
For citation:
Nikolaeva I.E., Plechev V.V., Mukhametyanov A.M., Biktashev R.M., Buzaev I.V., Khalikova G.A. Contrast Enhanced Echocardiography-Controlled Alcohol Septal Ablation for Hypertrophic Cardiomyopathy with Left Ventricular Outflow Tract Obstruction. Creative surgery and oncology. 2019;9(2):132-137. (In Russ.) https://doi.org/10.24060/2076-3093-2019-9-2-132-137


































