Перейти к:
Ангиографические методы в лечении пациентов с синдромом диабетической стопы
https://doi.org/10.24060/2076-3093-2021-11-4-300-306
Аннотация
Введение. Целью исследования явилось улучшение результатов лечения больных с синдромом диабетической стопы с помощью контроля инвазивного давления внутри артерии при рентгенохирургических вмешательствах.
Материалы и методы. В хирургическом отделении Клиники ФГБОУ ВО «БГМУ» Минздрава РФ за период с 2019 по 2020 г. пролечено 36 пациентов с сахарным диабетом 2-го типа и наличием гнойно-некротического поражения нижних конечностей. Из них 12 больных составили основную группу, в которой в комплекс лечебных мероприятий включен новый способ «Рентгенэндоваскулярное интраоперационное определение значимости стеноза артерий нижних конечностей» (Патент РФ RU 2737215 от 26.11.2020). Контрольную группу составили 24 пациента, получавших лечение без применения разработанного способа с соблюдением стандартов и рекомендаций необходимой помощи при данном заболевании.
Результаты и обсуждение. Ближайшие результаты лечения удалось оценить у всех пациентов основной и контрольной групп, вошедших в исследование. Оценка отдаленных результатов проводилась через 6, 12 и 24 месяца после выписки из стационара у 10 (83,3 %) пациентов основной группы и 19 (79,2 %) контрольной. В сроки до 2 лет конечность сохранена у 8 (66,7 %) больных с применением разработанной методики реваскуляризации и 10 (41,7 %) пациентов группы контроля (p < 0,05).
Заключение. Применение рентгенэндоваскулярных методов реваскуляризации конечности и способа интраоперационного определения значимости стеноза артерий нижних конечностей позволяют определить объем баллонной ангиопластики и подтвердить полноту реваскуляризации.
Ключевые слова
Для цитирования:
Галимов O.B., Ханов B.O., Ишметов В.Ш., Ибрагимов Т.Р., Биглова А.Ф., Суфияров Р.С. Ангиографические методы в лечении пациентов с синдромом диабетической стопы. Креативная хирургия и онкология. 2021;11(4):300-306. https://doi.org/10.24060/2076-3093-2021-11-4-300-306
For citation:
Galimov O.V., Khanov V.O., Ishmetov V.Sh., Ibragimov T.R., Biglova A.F., Sufiyarov R.S. Angiographic Therapies for Diabetic Foot Syndrome. Creative surgery and oncology. 2021;11(4):300-306. (In Russ.) https://doi.org/10.24060/2076-3093-2021-11-4-300-306
Введение
Сахарный диабет (СД) занимает лидирующие позиции среди всех заболеваний в России [1–5]. Им страдает около 8 млн человек, и заболевание является одной из основных причин ранней инвалидизации и смертности больных трудоспособного возраста. При этом у 20–80 % из общего числа больных с СД встречается развитие синдрома диабетической стопы с гнойно-некротическим поражением нижних конечностей [6–10].
В настоящее время проблемы, связанные с диабетической стопой, остаются наиболее частой причиной нетравматических ампутаций конечности, лишения трудоспособности, принося высочайший ущерб здоровью, снижая качество жизни больных и требуя больших материальных затрат для лечения и реабилитации пациентов [11–14]. Одной из задач при лечении данной категории больных является восстановление кровотока к нижней конечности. С целью ее реваскуляризации в первую очередь применяются рентгенэндоваскулярные методы [15–19].
Цель исследования: улучшить результаты лечения больных с синдромом диабетической стопы с помощью контроля инвазивного давления внутри артерии при рентгенохирургических вмешательствах.
Материал и методы
В хирургическом отделении Клиники ФГБОУ ВО «БГМУ» Минздрава России за период с 2019 по 2020 г. было пролечено 36 пациентов с сахарным диабетом 2-го типа и наличием гнойно-некротического поражения нижних конечностей (табл. 1).
|
Возраст |
Основная группа (n = 12) |
Контрольная группа (n = 24) |
||||||
|
м |
ж |
м |
ж |
|||||
|
абс. |
% |
абс. |
% |
абс. |
% |
абс. |
% |
|
|
40–49 |
- |
- |
2 |
16,7 |
2 |
8,3 |
2 |
8,3 |
|
50–59 |
2 |
16,7 |
1 |
8,3 |
2 |
8,3 |
4 |
16,7 |
|
60–69 |
2 |
16,7 |
3 |
25,0 |
4 |
16,7 |
6 |
25,0 |
|
70–77 |
1 |
8,3 |
1 |
8,3 |
1 |
4,2 |
3 |
12,5 |
|
Итого |
5 |
41,7 |
7 |
58,3 |
9 |
37,5 |
15 |
62,5 |
Таблица 1. Распределение пациентов исследуемых групп по возрасту и полу
Table 1. Cohort structure by age and gender
Из них 12 больных составили основную группу, в которой в комплекс лечебных мероприятий включен способ «Рентгенэндоваскулярное интраоперационное определение значимости стеноза артерий нижних конечностей», а также современные патогенетически обоснованные методы хирургического лечения. Контрольную группу составили 24 пациента, получавших лечение без применения разработанного комплексного подхода. Большую часть выборки составляли лица трудоспособного возраста, что свидетельствует о социально-экономической значимости проблемы.
Характеризуя клинический материал, необходимо отметить, что длительность заболевания при СД 2-го типа в 21 (58,3 %) случае была более 10 лет. Чаще всего трофические язвы приходились на возраст 50–59 и 60–69 лет — 9 (23,1 %) и 15 (41,7 %) случаев соответственно, что обусловлено увеличением лиц пожилого возраста в общем числе больных сахарным диабетом и увеличением средней продолжительности жизни. У 29 (80,6 %) пациентов отмечался нейроишемический тип поражения нижних конечностей и у 7 (19,4 %) смешанный.
В основной группе наблюдалось резкое снижение показателя парциального напряжения кислорода в коже стопы (Тср.О2), его среднее значение не превышало 19,3 ± 4,7 мм рт. ст., что является одним из объективных признаков диабетической ангиопатии в стадии критической ишемии нижней конечности.
Учитывая вариабельность поражения сосудистого русла при сахарном диабете, мы разработали способ (Патент РФ RU 2737215 от 26.11.2020), позволяющий четко выявлять локализацию наибольшего стенотического поражения стенки сосуда и, соответственно, определять эффективность ангиопластики, необходимость дополнять ее стентированием и контролировать восстановление гемодинамики в дистальных отделах сосудистого русла.
Способ выполняется во время проведения ангиографии. Основной задачей его является выполнение диагностики значимости стеноза при его условной безопасности, мобильности и способности к многократной интраоперационной воспроизводимости.
Технический результат достигается непосредственно при оперативном вмешательстве выполнением исследования в режиме реального времени, возможностью контроля после проведенных лечебных процедур в короткий промежуток времени с объективной оценкой значимости стеноза и его коррекции.
К внедрению данного способа нас побудили недостатки известных чрескожных и контактных УЗДС исследований, т. к. они имеют ограниченное использование на крупных кровеносных сосудах при «открытом» хирургическом вмешательстве на аорте, подвздошных, бедренных артериях. Нас же в большей степени интересуют меньшие по калибру артерии, а способ оценки стеноза при помощи ангиографии и компьютерной томографии с контрастированием не дает возможности определить конкретную локализацию стеноза, который приводит к ишемии конечности, при множественном поражении для более селективной баллонной ангиопластики.
Способ осуществляется следующим образом: во время проведения ангиографии в основной группе дополнительно производится измерение инвазивного давления в артериях нижних конечностей (рис. 1).
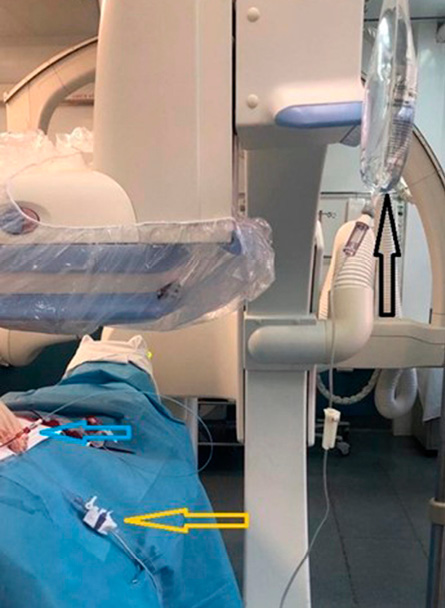
Рисунок 1. Система для измерения инвазивного давления (желтая стрелка — датчик инвазивного давления, синяя стрелка — катетер, черная стрелка — физиологический раствор с гепарином)
Figure 1. Invasive pressure monitoring appliance (invasive pressure sensor, yellow arrow; catheter, blue arrow; heparin saline, black arrow)
Посредством катетера с присоединенным датчиком инвазивного давления производили измерение до стенозов и после стенозов (рис. 2 А, Б).
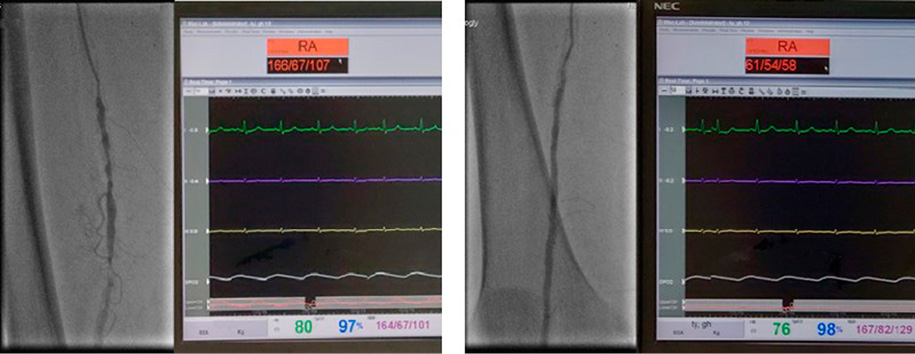
Рисунок 2. А — множественные гемодинамически значимые стенозы поверхностной бедренной артерии. Результат измерения инвазивного давления до стенозов; Б — результат измерения инвазивного давления после гемодинамически значимых стенозов (РКК у представленного случая составило 0,36)
Figure 2. A — multiple haemodynamically significant stenoses of superficial femoral artery. Pre-stenosis invasive pressure values; Б — invasive pressure after haemodynamically significant stenosis (limb blood flow reserve 0.36 in presented case)
Значимыми считались стенозы при систолическом градиенте давления >20 мм рт. ст. или при средним градиенте >10 мм рт. ст. в сочетании со снижением резерва кровотока конечности (РКК) ниже 1,0, который определяют как отношение давления за стенозом на фоне гиперемии и давления на неизменном участке перед стенозом.
До применения предложенного нами способа успехом выполнения баллонной ангиопластики артерий нижних конечностей считалось получение положительного рентгенохирургического результата, визуализируемого на контрольных снимках.
При использовании разработанного метода обязательным было сопоставление повторного измерения инвазивного давления в корригируемой артерии после баллонной ангиопластики с целью контроля успешности проведенного лечения.
Для этого также выполнялось измерение инвазивного артериального давления дистальнее и проксимальнее зоны баллоннной ангиопластики. Если средний градиент между полученными давлениями составлял более 20 мм рт. ст., то это свидетельствовало о неполноценной реваскуляризации и необходимости повторной баллонной ангиопластики и возможного стентирования пораженного участка артерии. Для полной достоверности производился подсчет РКК.
Если повторная баллонная ангиопластика приводила к удовлетворительным критериям артериального давления в корригируемом участке, то выполняли стентирование зоны баллонной ангиопластики с контрольным измерением инвазивного давления в сосуде проксимальнее и дистальнее стента (рис. 3).
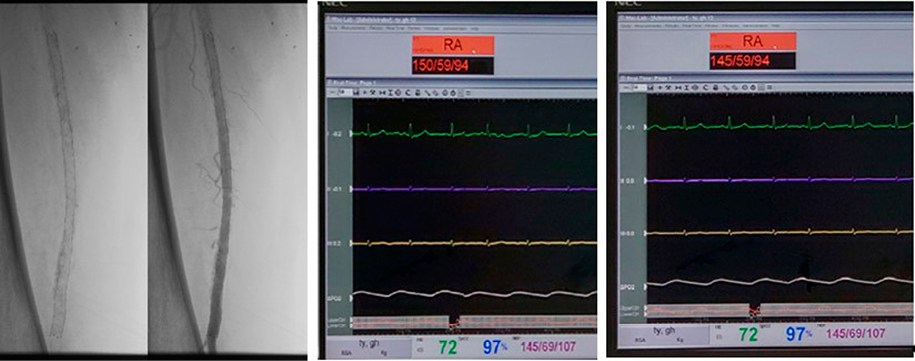
Рисунок 3. Результат стентирования зоны баллонной ангиопластики с контролем инвазивного давления до и после участка стентирования. Получен положительный ангиографический результат (РКК составил 0,95)
Figure 3. Balloon angioplasty zone stenting with invasive pressure control at both sides of stenting site. Positive angiography obtained (limb blood flow reserve 0.95)
В результате применения предложенного метода удалось вовремя точно скорректировать объем операции и достоверно улучшить кровоснабжение конечности, увеличив показатель РКК с 0,36 до 0,95.
Результаты и обсуждение
Ближайшие результаты лечения удалось оценить у всех пациентов основной и контрольной групп, вошедших в исследование. Необходимо отметить, что оценка результатов складывалась на основании анализа динамики клинических проявлений заболевания, выраженности и нивелирования симптоматики гнойно-воспалительного процесса, как местных проявлений, так и системных. Оценивалась динамика лабораторных данных, а также бактериологического, цитологического и морфологического исследований.
Одним из системных показателей купирования гнойного процесса является температурная реакция. Контроль температуры тела пациентов групп сравнения проводился ежедневно, при необходимости по часам в течение суток. В обеих группах отмечено последовательное снижение температуры тела до нормальных цифр, при этом в основной группе ее нормализация и стабилизация отмечались в среднем на 3,0 ± 0,9 суток (р < 0,01) быстрее, чем в группе контроля.
В основной группе на 3–5-е сутки отмечено стихание явлений перифокального воспаления, снижение количества раневого экссудата. В контрольной группе эти изменения наступали только на 6–7-е сутки. Основные показатели ближайших результатов представлены в таблице 2.
|
Показатель |
Основная группа |
Контрольная группа |
|
Полная эпителизация |
83,3 % |
58,3 % |
|
Средняя скорость эпителизации |
4,4 ± 1,3 см 2/нед. |
3,5 ± 1,15 см 2/нед. |
|
Ампутация конечности |
8,3 % |
12,5 % |
|
Количество некрэктомий на 1 больного |
1,5 |
2,1 |
|
Заживление дефектов без резекционных вмешательств |
16,7 % |
4,2 % |
Таблица 2. Показатели ближайших результатов лечения
Table 2. Immediate treatment outcomes
В основной группе удалось увеличить скорость эпителизации на 0,9 см 2/нед. (p < 0,01).
Комплексный подход с применением современных перевязочных покрытий, разработанного рентгенэндохирургического метода и декомпрессии нагрузки на стопу позволил уменьшить сроки лечения в среднем на 5,0 ± 3,9 суток (р < 0,001). При сравнении непосредственных результатов лечения в основной группе выявлено достоверное уменьшение ампутаций нижней конечности на уровне бедра (р < 0,05). Достоверно меньшим было количество некрэктомий в основной группе (р < 0,001) и, соответственно, меньшим оказалось число больных, которым выполнили несколько этапных операций (р < 0,05).
Оценка отдаленных результатов проводилась через 6, 12 и 24 месяца после выписки из стационара. Осмотр проводился в СКДЦ Клиники БГМУ. От 6 мес. до 2 лет результаты оценены у 10 (83,3 %) пациентов из основной группы и у 19 (79,2 %) контрольной.
Показатель сохранения опорной функции конечности через 6 мес. составил в основной группе 10 (83,3 %), в контрольной 17 (70,8 %) (p < 0,001). При этом 2 (16,7 %) пациентов основной группы и 5 (20,8 %) контрольной после осмотра в СКДЦ и проведения УЗДС были госпитализированы для определения возможности повторной реваскуляризации. При этом отмечено, что среди пациентов, использовавших декомпрессивную разгрузку стопы различными методами, рецидив получили лишь 3,9 % больных против 13,7 % человек, не следовавших рекомендациям (p < 0,01).
На данный период обследования 1 (8,3 %) пациент основной группы на фоне развития влажной гангрены стопы потерял конечность на уровне верхней трети бедра, в контрольной группе опорная функция утеряна в 4 (16,7 %) случаях (p < 0,05).
Летальный исход случился только в контрольной группе у 2 (8,3 %) пациентов вследствие сосудистых поражений других органов и систем, имеющих жизненно важное значение (ИМ, ОНМК и т. д.) (p < 0,05).
От 6 мес. до 1 года после рентгенэндоваскулярных вмешательств с применением разработанных методик отсутствие рецидива ишемии нижних конечностей отмечено у 8 (66,7 %) больных, проходимость сосудистого русла, в том числе в зоне коррекции, была сохранена у 13 (54,2 %) больных. К данному контрольному периоду высокая ампутация нижней конечности выполнена 2 (16,7 %) пациентам основной группы, 7 (29,2 %) контрольной (p < 0,01). Летальность составила в основной и контрольной группе 1 (8,3 %) и 3 (12,5 %) соответственно (p < 0,05).
Рецидив критической ишемии после реваскуляризации является следствием многофакторного комплекса вопросов, связанных не только с продолжающимся поражением сосудов в связи с основным заболеванием, но и комплаентностью пациента к требованиям врача по дисциплинированному, пожизненному выполнению определенных медикаментозных назначений, питанию и образу жизни.
В сроки от 1 до 2 лет конечность сохранена у 8 (66,7 %) больных с применением методик реваскуляризации и 10 (41,7 %) пациентов группы контроля (p < 0,05). Уменьшение динамики количества рецидивов и ампутаций может зависеть от компенсаторных способностей сосудистого русла нижней конечности к развитию коллатерального кровообращения.
Летальность за 2 года наблюдения составила 8,3 % (1 человек) в основной группе и 16,7 % (4 пациента) в контрольной (p < 0,05).
Заключение
Применение рентгенэндоваскулярных методов реваскуляризации конечности и способа интраоперационного определения значимости стеноза артерий нижних конечностей позволяет определить объем баллонной ангиопластики и подтвердить полноту реваскуляризации.
Внедрение разработанного способа позволило: достичь полного заживления пораженной стопы у 10 (83,3 %) пациентов основной группы; сократить в среднем количество некрэктомий с 2,1 до 1,5 операции (р < 0,05); увеличить среднюю скорость уменьшения площади язв на 0,90 ± 0,87 см 2/нед. (р < 0,01). Применение комплексных мероприятий в хирургическом лечении СДС позволило сохранить опорную функцию нижних конечностей к выписке из стационара у 11 (91,7 %) пациентов основной группы (р < 0,001), сократить сроки госпитализации в среднем на 5,0 ± 3,9 суток (р < 0,001), сократить в сроки до 2 лет количество ампутаций с 58,3 до 33,3 % (p < 0,05) и летальность с 16,7 до 8,3 % (p < 0,05).
Предложенный способ позволяет с высокой точностью определить значимый стеноз артерии и возможность выбора оперативного пособия в зоне значимого стеноза, обеспечить контроль адекватности вмешательства. Способ сопутствует коррекции нарушения гемодинамики, что дает преимущества в его повторяемости, мобильности, доступности и объективности полученных данных. Все эти факторы оказывают существенное влияние на улучшение результатов лечения пациентов данной категории
Информация о конфликте интересов. Конфликт интересов отсутствует.
Информация о спонсорстве. Данная работа не финансировалась.
Список литературы
1. Джемилова З.Н., Ситкин И.И., Сергеева С.В., Грачев П.В., Линьков К.Г., Лощенов В.Б. и др. Применение метода флуоресцентной ангиографии в ближнем инфракрасном диапазоне у пациента с сахарным диабетом и критической ишемией нижней конечности. Сахарный диабет. 2018;21(4):319–24. DOI: 10.14341/DM9764
2. Mohammedi K., Woodward M., Hirakawa Y., Zoungas S., Colagiuri S., Hamet P., et al. Presentations of major peripheral arterial disease and risk of major outcomes in patients with type 2 diabetes: results from the ADVANCE-ON study. Cardiovasc Diabetol. 2016;15(1):129. DOI: 10.1186/s12933-016-0446-x
3. Токмакова А.Ю., Егорова Д.Н., Доронина Л.П. Поражения нижних конечностей при сахарном диабете. Ожирение и метаболизм. 2017;14(1):41–7. DOI: 10.14341/omet2017141-47
4. Дедов И.И., Шестакова М.В., Майоров А.Ю., Викулова О.К., Галстян Г.Р., Кураева Т.Л. и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом. 9-й выпуск. Сахарный диабет. 2019;22(1S1):1–144. DOI: 10.14341/DM221S1
5. Aboyans V., Ricco J.B., Bartelink M.E.L., Björck M., Brodmann M., Cohnert T., et al. 2017 ESC Guidelines on the diagnosis and treatment of peripheral arterial diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteriesEndorsed by: the European Stroke Organization (ESO) Th e Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J. 2018;39(9):763–816. DOI: 10.1093/eurheartj/ehx095
6. Stoberock K., Kaschwich M., Nicolay S.S., Mahmoud N., Heidemann F., Rieß H.C., et al. Th e interrelationship between diabetes mellitus and peripheral arterial disease — a systematic review. Vasa. 2020:1–8. DOI: 10.1024/0301-1526/a000925
7. Сафаров С.Ю., Алиев М.А., Магомедов М.С., Сулейманов Ш.А., Султанова Р.С. Внедрение инновационных методов в комплексном лечении синдрома диабетической стопы. Вестник ДГМА. 2018;2:35–40.
8. Neupane S., Edla S., Maidona E., Sweet M.C., Szpunar S., Davis T., et al. Long-term outcomes of patients with diabetes mellitus undergoing percutaneous intervention for popliteal and infrapopliteal peripheral arterial disease. Catheter Cardiovasc Interv. 2018;92(1):117–23. DOI: 10.1002/ccd.27571
9. Ерошкин А.И., Кондрашин С.А., Терновой С.К., Васильев Д.Ю. КТ-ангиография нижних конечностей и КТ-перфузия стоп в диагностике, планировании и отслеживании результата реваскуляризации у пациента с синдромом диабетической стопы. REJR 2020;10(2):78–86. DOI: 10.21569/2222-7415-2020-10-2-78-86
10. Грекова Н.М., Лебедева Ю.В., Шишменцев Н.Б., Динерман Г.В. Пути снижения частоты высоких ампутаций при сахарном диабете и прогноз для оперированной диабетической стопы. Современные проблемы науки и образования. 2017;5. URL: http:// www.science-education.ru/ru/article/view?id=26714
11. Hischke S., Rieß H.C., Bublitz M.K., Kriston L., Schwaneberg T., Härter M., et al. Quality indicators in peripheral arterial occlusive disease treatment: a systematic review. Eur J Vasc Endovasc Surg. 2019;58(5):738–45. DOI: 10.1016/j.ejvs.2019.06.029
12. Шумилина М.В., Керен М.А., Хадзегова О.А. Индекс лодыжечного давления — первоочередной неинвазивный скрининг-тест для диагностики заболеваний артерий нижних конечностей: возможности и ограничения метода. Клиническая физиология кровообращения. 2020;17(3):183–8. DOI: 10.24022/1814-6910-2020-17-3-183-188
13. Butt T., Lilja E., Örneholm H., Apelqvist J., Gottsäter A., Eneroth M., et al. Amputation-free survival in patients with diabetes mellitus and peripheral arterial disease with heel ulcer: open versus endovascular surgery. Vasc Endovascular Surg. 2019;53(2):118–25. DOI: 10.1177/1538574418813746
14. Pourghaderi P., Yuquimpo K.M., RoginskiGuetter C., Mansfi eld L., Park H.S. Outcomes following lower extremity amputation in patients with diabetes mellitus and peripheral arterial disease. Ann Vasc Surg. 2020;63:259–68. DOI: 10.1016/j.avsg.2019.08.084
15. Белик Б.М., Чумбуридзе И.П., Штильман М.Ю., Явруян О.А., Савченко Ю.П. Комплексное лечение больных с гнойнонекротическими осложнениями при нейропатической форме синдрома диабетической стопы Хирургия. Журнал им. Н.И. Пирогова. 2020;4:81–7. DOI: 10.17116/hirurgia202004181
16. Yang S.L., Zhu L.Y., Han R., Sun L.L., Li J.X., Dou J.T. Pathophysiology of peripheral arterial disease in diabetes mellitus. J Diabetes. 2017;9(2):133–40. DOI: 10.1111/1753-0407.12474
17. Бурлева Е.П., Бабушкина Ю.В., Галимзянов Ф.В., Фоминых А.Н. Результаты дифференцированного лечения пациентов с синдромом диабетической стопы на этапе специализированной хирургической помощи. Хирургия. Журналим. Н.И. Пирогова. 2019;5:42–51. DOI: 10.17116/hirurgia201905142
18. Loja M.N., Brunson A., Li C.S., Carson J.G., White R.H., Romano P.S., et al. Racial disparities in outcomes of endovascular procedures for peripheral arterial disease: an evaluation of California hospitals, 2005–2009. Ann Vasc Surg. 2015;29(5):950–9. DOI: 10.1016/j.avsg.2015.01.006
19. Кавтеладзе З.А., Пюмпюлян А.Г., Ермолаев П.М., Даниленко С.Ю., Завалишин С.Е., Асатрян К.В., и др. Возможности эндоваскулярной хирургии. Эндоваскулярное лечение окклюзированных артерий голени после множественных сосудистых вмешательств. Эндоваскулярная хирургия. 2020;7(1):94–100. DOI: 10.24183/2409-4080-2020-7-1-94-100
Об авторах
O. B. ГалимовРоссия
Галимов Олег Владимирович, д.м.н., профессор, кафедра хирургических болезней и новых технологий с курсом ИДПО
Республика Башкортостан, Уфа
B. O. Ханов
Россия
Ханов Владислав Олегович, д.м.н., профессор, кафедра хирургических болезней и новых технологий с курсом ИДПО
Республика Башкортостан, Уфа
В. Ш. Ишметов
Россия
Ишметов Владимир Шамильевич, д.м.н., профессор, кафедра госпитальной хирургии
Республика Башкортостан, Уфа
Т. Р. Ибрагимов
Россия
Ибрагимов Теймур Рамиз оглы, кафедра хирургических болезней и новых технологий с курсом ИДПО
Республика Башкортостан, Уфа
А. Ф. Биглова
Россия
Биглова Айгуль Фанилевна, кафедра хирургических болезней и новых технологий с курсом ИДПО
Республика Башкортостан, Уфа
Р. С. Суфияров
Россия
Суфияров Ринат Сабитович, д.м.н., профессор, кафедра хирургических болезней и новых технологий с курсом ИДПО
Республика Башкортостан, Уфа
Рецензия
Для цитирования:
Галимов O.B., Ханов B.O., Ишметов В.Ш., Ибрагимов Т.Р., Биглова А.Ф., Суфияров Р.С. Ангиографические методы в лечении пациентов с синдромом диабетической стопы. Креативная хирургия и онкология. 2021;11(4):300-306. https://doi.org/10.24060/2076-3093-2021-11-4-300-306
For citation:
Galimov O.V., Khanov V.O., Ishmetov V.Sh., Ibragimov T.R., Biglova A.F., Sufiyarov R.S. Angiographic Therapies for Diabetic Foot Syndrome. Creative surgery and oncology. 2021;11(4):300-306. (In Russ.) https://doi.org/10.24060/2076-3093-2021-11-4-300-306


































