Перейти к:
Клинический случай стентирования коронарной артерии под контролем ВСУЗИ у больного с хронической почечной недостаточностью
https://doi.org/10.24060/2076-3093-2023-13-4-342-347
Аннотация
Введение. В условиях расширения показаний к ЧКВ у больных ишемической болезнью сердца с тяжелой сопутствующей патологией растет число пациентов с хронической почечной недостаточностью. КИН является одним из грозных осложнений, что не только усугубляет течение основного заболевания, но и уменьшает продолжительность жизни больного. Современные методы внутрисосудистой визуализации широко внедряются в реальную клиническую практику эндоваскулярной хирургии. В условиях растущего числа выполняемых ЧКВ у больных с тяжелой сопутствующей патологией использование ВСУЗИ улучшит не только качество выполняемых стентирований, но и снизит риски развития КИН ввиду уменьшения объема вводимого контраста. Материалы и методы. Приводим клинический случай стентирования правой коронарной артерии без использования контрастного вещества под контролем ВСУЗИ у пациентки с хронической болезнью почек и диагнозом: Ишемическая болезнь сердца. Стенокардия напряжения, III функциональный класс (одышка как эквивалент). Баллонная ангиопластика и стентирование ОВ и ПМЖВ. Гиперлипидемия 2 а. Атеросклероз аорты, брахиоцефальных и коронарных артерий. Гипертоническая болезнь III стадии. Контролируемая артериальная гипертензия. Риск ССО IV. Сахарный диабет 2 типа. Целевой уровень гликированного гемоглобина менее 7,5 %. Ожирение 2 степени, экзогенно-конституциональное. Микролиты почек. ХБП 4 стадия (СКФ 29 мл/мин/1,73 м 2). Цереброваскулярная болезнь. Хроническая ишемия головного мозга. Результаты и обсуждение. В описанном клиническом случае удалось добиться полной реваскуляризации миокарда под контролем ВСУЗИ с использованием минимального количества контрастного препарата у больного с тяжелой ХПН Данный клинический пример демонстрирует преимущество малоинвазивных эндоваскулярных вмешательств у сложной категории больных, которые позволят расширить возможности оказания высокотехнологичной помощи больным, имеющим значительные ограничения в применении контрастных препаратов ввиду тяжелой ХПН с высоким риском развития КИН. Заключение. На сегодняшний день все большее количество рентгеноперационных страны оснащены внутрисосудистыми модальностями, что, безусловно, приведет к более широкому их применению. Навыки и знания применения ВСУЗИ позволят в меньшем объеме использовать РКП, что приведет к снижению риска развития КИН и, как следствие, улучшению прогноза пациентов со сниженной функцией почек и высоким риском КИН.
Ключевые слова
Для цитирования:
Васильев Д.К., Руденко Б.А., Фещенко Д.А., Шукуров Ф.Б., Шаноян А.С. Клинический случай стентирования коронарной артерии под контролем ВСУЗИ у больного с хронической почечной недостаточностью. Креативная хирургия и онкология. 2023;13(4):342-347. https://doi.org/10.24060/2076-3093-2023-13-4-342-347
For citation:
Vasiliev D.K., Rudenko B.A., Feshchenko D.A., Shukurov F.B., Shanoyan A.S. Clinical Case of IVUS-Guided Coronary Artery Stenting in a Patient with Chronic Renal Failure. Creative surgery and oncology. 2023;13(4):342-347. (In Russ.) https://doi.org/10.24060/2076-3093-2023-13-4-342-347
ВВЕДЕНИЕ
В течение последних лет увеличилось количество проводимых чрескожных коронарных вмешательств (ЧКВ) с использованием рентгеноконтрастных препаратов (РКП) [1]. Благодаря увеличению средней продолжительности жизни населения увеличилась доля пациентов с коморбидной патологией, в частности с хронической болезнью почек (ХБП). Данная группа пациентов нередко вызывает серьезные технические сложности при проведении ЧКВ и имеет более тяжелое атеросклеротическое поражение коронарного русла [2][3]. У пациентов с ХБП поводом для выполнения ЧКВ часто служит возникновение нестабильной стенокардии или инфаркта миокарда [4], и, безусловно, наличие ХБП служит предиктором развития неблагоприятных коронарных событий в будущем [5][6]. При этом будущий прогноз в основном определяется развитием контраст-индуцированной нефропатии (КИН) [7]. У пациентов с ХБП, которым планируется ЧКВ, всегда существует высокий риск развития КИН. В сложившейся ситуации необходимо применять все меры по снижению использования РКП при ЧКВ для профилактики развития КИН. Одним из решений проблемы развития КИН после ЧКВ может стать использование внутрисосудистого ультразвука (ВСУЗИ), для работы которого не требуется введение РКП. В реальной клинической практике стентирование коронарной артерии под контролем ВСУЗИ без контрастных веществ возможно провести при неосложненных стенотических поражениях и при обычной анатомии коронарного русла. ВСУЗИ дает более расширенное представление о морфологии поражения коронарного русла, сосудистой архитектоники и для выбора метода и тактики проведения ЧКВ.
МАТЕРИАЛЫ И МЕТОДЫ
Описание клинического случая
Пациентка С., 69 лет, поступила в отделение рентгенхирургических методов диагностики и лечения ФГБУ «НМИЦ ТПМ» Минздрава России в октябре 2022 года с жалобами на чувство нехватки воздуха при подъеме по лестнице на 1 этаж, эпизоды повышения артериального давления до максимального значения 200/100 мм рт. ст. В анамнезе артериальная гипертензия в течение 20 лет, сахарный диабет с 2012 года; инфаркт миокарда и нарушение мозгового кровообращения в анамнезе отрицает. Длительно беспокоит одышка и чувство нехватки воздуха при ходьбе с постепенным прогрессированием. В последние месяцы чувство нехватки воздуха возникает при подъеме по лестнице на 1 этаж.
По данным эхокардиографии: фракция выброса сохранная, нарушений локальной сократимости и клапанной патологии нет, дилатации полостей нет. В марте 2022 года проводился скрининг коронарного кальция с определением коронарного кальция — кальциевый индекс по Аgatston 1077 ед. Амбулаторно выполнена нагрузочная проба — результат сомнительный.
В июле 2022 г. госпитализирована в клинику центра. Пациентке выполнена коронарная ангиография: ствол левой коронарной артерии не изменен, в передней межжелудочковой артерии протяженный 90 % стеноз в проксимальном сегменте, стеноз 90 % в огибающей ветви, 90 % стеноз в проксимальном сегменте правой коронарной артерии (ПКА), окклюзия задней межжелудочковой ветви. Учитывая выявленное многососудистое поражение коронарного русла и наличие сахарного диабета, с целью определения дальнейшей тактики лечения пациентка консультирована сердечно-сосудистым хирургом. Было рекомендовано проведение аортокоронарного шунтирования, однако пациентка категорически отказалась и написала письменный отказ от операции. Больная была консультирована рентген-эндоваскулярным хирургом центра. Рекомендовано поэтапное стентирование коронарного русла. Первым этапом выполнено ЧКВ в бассейне передней межжелудочковой артерии и огибающей ветви без каких-либо технических сложностей.
Целью текущей госпитализации послужило выполнение следующего этапа реваскуляризации — ЧКВ в бассейне ПКА. В настоящее время принимает клопидогрель 75 мг, бисопролол 7,5 мг, амлодипин 10 мг, лозартан 50 мг, метформин 3,0 гр\сут, диабетон 120 мг\сут, розувастатин 40 мг. На основании данных жалоб, анамнеза, физикального и инструментального обследований выставлен клинический диагноз: Ишемическая болезнь сердца. Стенокардия напряжения III функциональный класс (одышка как эквивалент). Баллонная ангиопластика и стентирование ОВ и ПМЖВ. Гиперлипидемия 2 а. Атеросклероз аорты, брахиоцефальных и коронарных артерий. Гипертоническая болезнь III стадии. Контролируемая артериальная гипертензия. Риск ССО IV. Сахарный диабет 2 типа. Целевой уровень гликированного гемоглобина менее 7,5 %. Ожирение 2 степени, экзогенно-конституциональное. Микролиты почек. ХБП 4 стадия (СКФ 29 мл/мин/1,73 м 2). Цереброваскулярная болезнь. Хроническая ишемия головного мозга.
В рамках подготовки к операции выполнен комплекс лабораторных обследований. В биохимическом анализе крови обратило на себя внимание повышение креатинина до 155,0 мкмоль/л, скорость клубочкой фильтрации составила СКФ 29 мл/мин/1,73 м2. Таким образом, пациенту с ХБП и высоким риском развития КИН принято решение о проведении эндоваскулярной реваскуляризации ПКА без использования контрастного вещества под контролем ВСУЗИ. Пациентка была консультирована врачом-нефрологом, даны рекомендации по предоперационной подготовке к ЧКВ. Для снижения риска развития КИН использовался изоосмолярный РКП йодиксанол.
Под местной анестезией произведена пункция правой лучевой артерии по Сельдингеру. Установлен интродьюсер 6F. Для навигации использована ангиография ПКА, выполненная ранее (рис. 1).
Катетер-гид установлен в устье ПКА. Первый коронарный проводник заведен в дистальный сегмент ПКА. Второй коронарный проводник заведен в восходящую аорту для исключения глубокой интубации артерии кончиком катетера-гида и дополнительной навигации устья ПКА (рис. 2).
Выполнено ВСУЗИ, по данным которого в проксимальном сегменте ПКА выявлено кальцинированное 90 % атеросклеротическое поражение, длина пораженного сегмента составила 34 мм, диаметр пораженного сосуда 2,8 мм. Выполнена предилатация стенозированного участка ПКА баллонными катетерами Sprinter Legend 2,25×15 мм и Trek 2,75×20 мм инфляцией до 12 атм (рис. 3).
Выполнено контрольное ВСУЗИ, по результатам которого данных о наличии диссекции и тромбоза не получено, остаточный стеноз составил 50 %. В область остаточного стеноза ПКА позиционирован и имплантирован стент с лекарственным покрытием 3×38 мм инфляцией 12 атм (рис. 4).
Выполнена постдилатация стентированного сегмента ПКА некомплаенсным баллонным катетером 3×15 мм инфляцией 20 атм (рис. 5).
Выполнено ВСУЗИ стентированного сегмента ПКА, по данным которого визуализируется полная аппозиция стента, остаточного стеноза нет. На контрольной съемке с использованием 2,5 мл контрастного вещества стент полностью расправлен, признаков диссекции нет, остаточного стеноза нет, кровоток в артерии TIMI-3 (рис. 6).
Интродьюсер из правой лучевой артерии извлечен. Гемостаз. Наложена давящая асептическая повязка. Операция прошла без осложнений. Послеоперационный период протекал без особенностей. Ангинозные боли не рецидивировали. Пациентка была выписана на следующий день после операции под наблюдение кардиолога по месту жительства. Ей даны рекомендации по диете, соблюдению режима труда и отдыха, назначена оптимальная медикаментозная терапия.
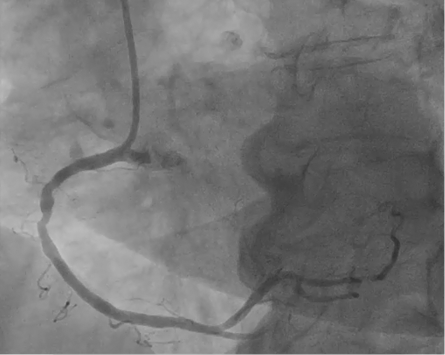
Рисунок 1. Ангиография ПКА от мая 2022 г.
Figure 1. RCA angiography, May 2022
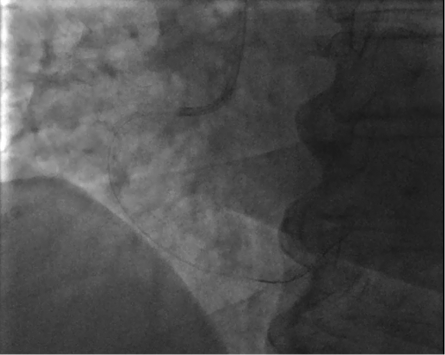
Рисунок 2. Коронарный проводник в дистальном сегменте ПКА
Figure 2. Coronary guidewire in the distal segment of the PCA
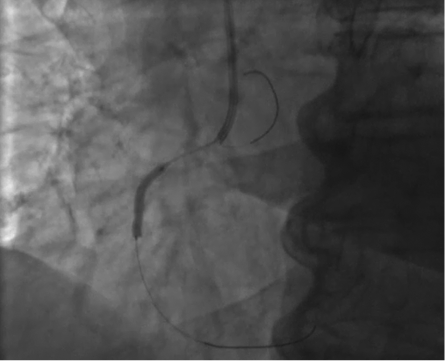
Рисунок 3. Предилатация зоны поражения ПКА
Figure 3. Predilation in the area of PCA lesion
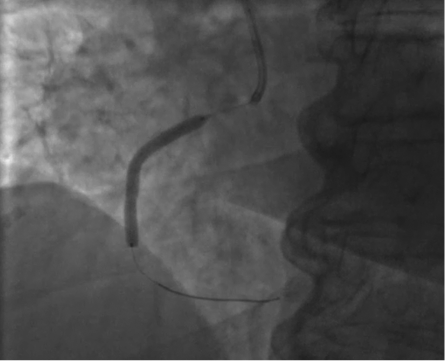
Рисунок 4. Имплантация стента с лекарственным покрытием в зоне поражения ПКА
Figure 4. Drug-eluting stent implantation in the area of PCA lesion
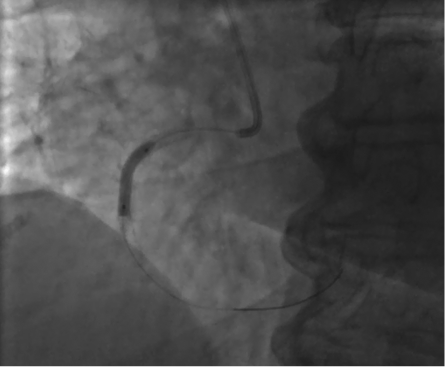
Рисунок 5. Постдилатация стентированного участка ПКА
Figure 5. Postdilation in the stented area of the PCA
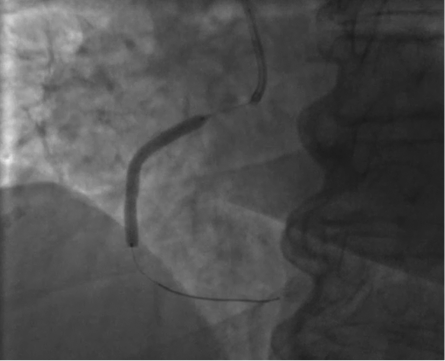
Рисунок 6. Финальная ангиография ПКА
Figure 6. Final angiography of the PCA
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
КИН — острое повреждение почек, возникающее после внутрисосудистого введения йодсодержащего РКП [8][9]. Несмотря на использование современных изоосмолярных РКП, риск КИН остается значительным, особенно среди пациентов с предшествующим нарушением функции почек [10]. В патогенезе острого повреждения почек при применении РКП лежат два основных механизма: нарушение почечной гемодинамики, что ведет к вазоконстрикции и ишемии коркового слоя почки; прямое токсическое действие РКП на эпителиальные клетки канальцев. КИН диагностируется при наличии повышения креатинина сыворотки на ≥26,5 мкмоль/л от исходного уровня в течение 48 часов или повышения креатинина сыворотки в 1,5 раза по сравнению с известным исходным уровнем в течение недели до исследования. Клиническое течение КИН зависит от исходной функции почек, сопутствующих факторов риска, степени гидратации и других факторов. Обычно КИН проявляется бессимптомным повышением сывороточного креатинина в течение 24–48 часов после внутрисосудистого введения РКП, достигает максимума через 3–5 дней и возвращается к исходному уровню через 7–10 дней.
Для определения риска развития КИН у кардиологических пациентов перед чрескожным коронарным вмешательством используется шкала Mehran [11]. Она позволяет предсказать риск развития КИН и необходимость использования гемодиализа [12].
Согласно шкале Mehran пациентка имела риск развития КИН 14 %, необходимость проведения гемодиализа 0,12 %. В представленном клиническом случае пациентка имела высокий риск развития КИН, что потребовало минимизировать объем вводимого РКП во время эндоваскулярной реваскуляризации ПКА. Безусловно, не у всех пациентов, которые имеют высокий риск КИН, возможно выполнение ЧКВ без РКП. В приведенном клиническом случае анатомия ПКА была известна, так как ранее уже выполнялась коронарная ангиография. ПКА имеет прямой линейный ход и малое количество ответвлений, что упрощает навигацию и минимизирует риск острого закрытия боковой ветки. Прямолинейный ход артерии позволяет без серьезных проблем завести коронарный проводник в дистальное русло без использования РКП. Второй коронарный проводник, заведенный в восходящую аорту, позволяет исключить глубокую интубацию артерии проводниковым катетером и дает дополнительный контроль за расположением устья ПКА. Использование ВСУЗИ позволяет контролировать процесс на каждом этапе операции, выбирать диаметр баллонного катетера для предилатации, диаметр и длину стента и контроль после имплантации стента.
ЗАКЛЮЧЕНИЕ
В условиях расширения показаний к ЧКВ у больных ишемической болезнью сердца с тяжелой сопутствующей патологией растет число пациентов с хронической почечной недостаточностью. Увеличение количества ЧКВ требует активного внедрения новых методов внутрисосудистой визуализации, которые позволят минимизировать введение больших объемов РКП и таким образом снизят риск развития КИН. Развитие КИН имеет серьезные прогностические последствия, которые связаны с увеличением длительности пребывания в стационаре, высокой частотой сердечно-сосудистых и неврологических событий, более высокими показателями госпитальной, годовой и 5-летней летальности [13–15]. Использование современных методов внутрисосудистой визуализации, ВСУЗИ в частности, позволяет безопасно и эффективно проводить реваскуляризацию в группе высокого риска развития КИН.
На сегодняшний день все большее количество рентгеноперационных страны оснащены внутрисосудистыми модальностями, что, безусловно, приведет к более широкому их применению. Навыки и знания применения ВСУЗИ позволят в меньшем объеме использовать РКП, что приведет к снижению риска развития КИН и, как следствие, улучшению прогноза пациентов со сниженной функцией почек и высоким риском КИН.
Информированное согласие. Информированное согласие пациента на публикацию своих данных получено.
Statement of informed consent. Written informed consent was obtained from the patient for publication of this case report and accompanying materials.
Информация о конфликте интересов. Конфликт интересов отсутствует.
Conflict of interest. The authors declare no conflict of interest.
Информация о спонсорстве. Данная работа не финансировалась.
Sponsorship data. This work is not funded.
Список литературы
1. Алекян Б.Г., Григорьян А.М., Стаферов А.В., Карапетян Н.Г. Рентгенэндоваскулярная диагностика и лечение заболеваний сердца и сосудов в Российской Федерации — 2020 год. Эндоваскулярная хирургия. 2021;8(Спец. вып.):S5–248. DOI: 10.24183/2409-4080-2021-8S-S5-S248
2. Sarnak M.J., Amann K., Bangalore S., Cavalcante J.L., Charytan D.M., Craig J.C., et al. Chronic kidney disease and coronary artery disease: JACC state-of-the-art review. J Am Coll Cardiol. 2019;74(14):1823–38. DOI: 10.1016/j.jacc.2019.08.1017
3. Дунаева А.Р., Щербакова А.С., Хафизов Е.Н., Загидуллин Н.Ш. Контраст-индуцированная нефропатия при коронарографии. Практическая медицина. 2014;3(79):35–40.
4. Holzmann M.J., Siddiqui A.J. Outcome of percutaneous coronary intervention during non-ST-segment-elevation myocardial infarction in elderly patients with chronic kidney disease. J Am Heart Assoc. 2020;9(12):e015084. DOI: 10.1161/JAHA.119.015084
5. Gupta T., Paul N., Kolte D., Harikrishnan P., Khera S., Aronow W.S., et al. Association of chronic renal insufficiency with in-hospital outcomes after percutaneous coronary intervention. J Am Heart Assoc. 2015;4(6):e002069. DOI: 10.1161/JAHA.115.002069
6. Guo W., Song F., Chen S., Zhang L., Sun G., Liu J., et al. The relationship between hyperuricemia and contrast-induced acute kidney injury undergoing primary percutaneous coronary intervention: secondary analysis protocol for the ATTEMPT RESCIND-1 study. Trials. 2020;21(1):567. DOI: 10.1186/s13063-020-04505-w
7. Sun G., Chen P., Wang K., Li H., Chen S., Liu J., et al. Contrast-induced nephropathy and long-term mortality after percutaneous coronary intervention in patients with acute myocardial infarction. Angiology. 2019;70(7):621–6. DOI: 10.1177/0003319718803677
8. Faucon A.L., Bobrie G., Clément O. Nephrotoxicity of iodinated contrast media: From pathophysiology to prevention strategies. Eur J Radiol. 2019;116:231–41. DOI: 10.1016/j.ejrad.2019.03.008
9. Khwaja A. KDIGO clinical practice guidelines for acute kidney injury. Nephron Clin Pract. 2012;120(4):c179–84. DOI: 10.1159/000339789
10. Rihal C.S., Textor S.C., Grill D.E., Berger P.B., Ting H.H., Best P.J., et al. Incidence and prognostic importance of acute renal failure after percutaneous coronary intervention. Circulation. 2002;105(19):2259–64. DOI: 10.1161/01.cir.0000016043.87291.33
11. Mehran R., Aymong E.D., Nikolsky E., Lasic Z., Iakovou I., Fahy M., et al. A simple risk score for prediction of contrast-induced nephropathy after percutaneous coronary intervention: development and initial validation. J Am Coll Cardiol. 2004;44(7):1393–9. DOI: 10.1016/j.jacc.2004.06.068
12. Hoste E.A., De Waele J.J., Gevaert S.A., Uchino S., Kellum J.A. Sodium bicarbonate for prevention of contrast-induced acute kidney injury: a systematic review and meta-analysis. Nephrol Dial Transplant. 2010;25(3):747–58. DOI: 10.1093/ndt/gfp389
13. Rufino Hernández J.M., Zamora Rodríguez N., Rodríguez Adanero C., Lorenzo Sellares V., Torres A. Acute renal failure in a tertiary referal hospital, a relevant cause of chronic renal failure and mortality. Nefrologia. 2017;37(6):657–8. DOI: 10.1016/j.nefro.2017.03.008
14. Ikizler T.A., Parikh C.R., Himmelfarb J., Chinchilli V.M., Liu K.D., Coca S.G., et al. A prospective cohort study of acute kidney injury and kidney outcomes, cardiovascular events, and death. Kidney Int. 2021;99(2):456–65. DOI: 10.1016/j.kint.2020.06.032
15. Ronco F., Tarantini G., McCullough P.A. Contrast induced acute kidney injury in interventional cardiology: an update and key guidance for clinicians. Rev Cardiovasc Med. 2020;21(1):9–23. DOI: 10.31083/j.rcm.2020.01.44
Об авторах
Д. К. ВасильевРоссия
Васильев Дмитрий Константинович — м.н.с., отдел инновационных методов профилактики, диагностики и лечения сердечно-сосудистых и других хронических неинфекционных заболеваний, отделение рентгенэндоваскулярных методов диагностики и лечения
Москва
Б. А. Руденко
Россия
Руденко Борис Александрович — д.м.н., отдел инновационных методов профилактики, диагностики и лечения сердечно-сосудистых и других хронических неинфекционных заболеваний, отделение рентгенэндоваскулярных методов диагностики и лечения
Москва
Д. А. Фещенко
Россия
Фещенко Дарья Анатольевна — отделение рентгенэндоваскулярных методов диагностики и лечения, операционный блок
Москва
Ф. Б. Шукуров
Россия
Шукуров Фирдавс Баходурович — отделение рентгенэндоваскулярных методов диагностики и лечения
Москва
А. С. Шаноян
Россия
Шаноян Артем Сергеевич — к.м.н., отделение рентгенхирургических методов диагностики и лечения
Москва
Рецензия
Для цитирования:
Васильев Д.К., Руденко Б.А., Фещенко Д.А., Шукуров Ф.Б., Шаноян А.С. Клинический случай стентирования коронарной артерии под контролем ВСУЗИ у больного с хронической почечной недостаточностью. Креативная хирургия и онкология. 2023;13(4):342-347. https://doi.org/10.24060/2076-3093-2023-13-4-342-347
For citation:
Vasiliev D.K., Rudenko B.A., Feshchenko D.A., Shukurov F.B., Shanoyan A.S. Clinical Case of IVUS-Guided Coronary Artery Stenting in a Patient with Chronic Renal Failure. Creative surgery and oncology. 2023;13(4):342-347. (In Russ.) https://doi.org/10.24060/2076-3093-2023-13-4-342-347
JATS XML


































