Перейти к:
Острая спаечная кишечная непроходимость: сравнительный анализ открытых и лапароскопических операций
https://doi.org/10.24060/2076-3093-2022-12-1-35-42
Аннотация
Введение. Острая спаечная кишечная непроходимость (ОСКН) является одной из частых причин в экстренной хирургии, требующих выполнения неотложных оперативных вмешательств. ОСКН — наиболее частое показание как для резекции тонкой кишки, так и для адгезиолизиса. В 60 % причиной обструкции тонкой кишки являются послеоперационные спайки.
Материалы и методы. Представлен анализ результатов лечения 197 больных с острой спаечной кишечной непроходимостью, из которых 63 пациентам была выполнена экстренная лапаротомия, 134 — планировали лапароскопические операции. В обследовании применяли физикальные, лабораторные, лучевые методы исследования (обзорная рентгенография живота, УЗИ, КТ), лапароскопию, мониторинг внутрибрюшного давления.
Результаты и обсуждение. Из 134 пациентов, запланированных на лапароскопический адгезиолизис, только у 46,2 % операция завершена лапароскопически, в 53,8 % потребовалась конверсия на лапаротомию. Основными причинами конверсии были массивный спаечный процесс, интраоперационная нестабильность гемодинамики, потребность в декомпрессии кишечника, редко — осложнения. При лапароскопических операциях отметили снижение частоты хирургических осложнений по сравнению с лапаротомией (6,4 и 12,69 %), летальности (6 и 6,3 %), сроков госпитализации (6,5 и 12 дней), сокращение продолжительности операций (75 и 118 минут соответственно).
Заключение. Хирургическое лечение лапароскопическим методом больных с острой спаечной кишечной непроходимостью возможно у 31,47 % к их общему числу, в 46,2 % — после диагностической лапароскопии, но требуется тщательный отбор больных на лапароскопический адгезиолизис. Прежде всего необходимо оценить тяжесть состояния больных, стабильность гемодинамики, выраженность спаечного процесса и коморбидной кардиореспираторной патологии. Показанием к лапароскопическим операциям является спаечный процесс I– II степени.
Ключевые слова
Для цитирования:
Тимербулатов Ш.В., Сибаев В.М., Тимербулатов В.М., Забелин М.В., Тимербулатов М.В., Сагитов Р.Б., Гафарова А.Р. Острая спаечная кишечная непроходимость: сравнительный анализ открытых и лапароскопических операций. Креативная хирургия и онкология. 2022;12(1):35-42. https://doi.org/10.24060/2076-3093-2022-12-1-35-42
For citation:
Timerbulatov Sh.V., Sibaev V.M., Timerbulatov V.M., Zabelin M.V., Timerbulatov M.V., Sagitov R.B., Gafarova A.R. Acute Adhesive Small Bowel Obstruction: a Comparative Analysis of Open and Laparoscopic Surgery. Creative surgery and oncology. 2022;12(1):35-42. (In Russ.) https://doi.org/10.24060/2076-3093-2022-12-1-35-42
Введение
Острая спаечная кишечная непроходимость (ОСКН) является одной из частых причин в экстренной хирургии, требующих выполнения неотложных оперативных вмешательств [1–4].
ОСКН — наиболее частое показание как для резекции тонкой кишки, так и для адгезиолизиса [3].
В 60 % причиной обструкции тонкой кишки являются послеоперационные спайки [1].
Сроки госпитализации пациентов колеблются от 8 до 16 дней при хирургическом лечении, около 5 — при консервативном, госпитальная летальность — от 3 до 7 % [5–7].
При хирургическом лечении ОСКН до настоящего времени золотым стандартом были открытые операции (ОО), в последние десятилетия альтернативой лапаротомии становятся лапароскопические операции [8–10], хотя преимущества последних остаются неопределенными [11].
Возможности лапароскопического адгезиолизиса (ЛСАЛ) во многом зависят от характера осложнения (наличие странгуляции, ишемии кишечника), распространенности, морфологических характеристик брюшинных спаек, что находит отражение в классификациях спаек брюшной полости.
Наиболее известной является классификация H.V. Zuhlke и др. [12], основанная на выраженности и некоторых морфологических особенностях спаек: 0-я степень — отсутствие или незначительные спайки; 1-я степень — спайки в виде пленки, легко отделяются тупым способом; 2-я степень — возможно разделение тупым путем или частично острым путем, четкая васкуляризация спаек; 3-я степень — возможно рассечение только острым путем, четкая васкуляризация спаек, 4-я степень — иссечение только острым путем, плотные спайки, трудно предотвратить повреждение органов.
В соответствии с системой оценки распространенности спаек — так называемым индексом перитонеальный адгезии (ИПА) [13], выраженность спаечного процесса определяют по шкале до 3 баллов и локализации в брюшной полости (10 участков): степень адгезии: 0-я степень — отсутствие спаек; 1-я степень — пленчатые спайки, рассечение острым путем; 2-я степень — выраженные спайки, рассечение острым путем; 3-я степень — выраженные спайки с васкуляризацией, рассечение только острым путем. Области брюшной полости: А — правый верхний квадрант; В — эпигастрий; С — левый верхний квадрант; D — левая боковая область; E — левый нижний квадрант; F — тазовая область; G — правый нижний квадрант; Н — правая боковая область; I — центральный квадрант.
Как видно, обе классификации основаны на оценке спаечного процесса как по морфологической картине, так и по распространенности, интраоперационно, что существенно снижает их клиническую значимость, и чаще всего могут служить для определения возможностей лапароскопического завершения оперативных вмешательств.
Цель исследования — изучить результаты применения лапароскопических вмешательств в лечении пациентов с острой спаечной кишечной непроходимостью сравнительно с открытыми операциями.
Материал и методы
За 2014–2019 гг. в клинику было госпитализировано 197 больных по поводу ОСКН, из них 63 после предоперационный подготовки были выполнены открытые оперативные вмешательства (31,9 %), остальным 134 планировались лапароскопические операции (68,1 %). В последней группе дети составили 17,16 % (n = 23), лица старше 18 лет — 82,84 % (n = 111).
Обследование больных с ОСКН проводилось в соответствии с национальными клиническими рекомендациями [14]. Обзорная рентгенография живота применялась во всех случаях. При выявлении чаш Клойбера, кишечных арок, выраженной пневматизации тонкой кишки в сочетании с яркой клинической картиной (частая рвота, отсутствие газов, стула), наличии выпота в брюшной полости, признаках гиповолемии диагноз ОСКН не вызывает сомнения и возникают показания к оперативному лечению. При ранних сроках лечения диагностический процесс часто затягивается. В таких случаях проводили контроль пассажа контрастного препарата по кишечнику с рентгенографией живота через 2–3, 6 и 8 часов. При поступлении всем больным наряду с обзорной рентгенографией живота проводили УЗИ органов брюшной полости.
При консервативном лечении через 6 часов повторно определяли уровень электролитов крови. Дополнительно к общепринятым методам исследования при госпитализации и через каждые 6 часов измеряли внутрибрюшное давление в мочевом пузыре [15] аппаратом «Тритон-1500» или манометром собственной конструкции (Патент РФ № 81629. Манометр для измерения интраабдоминального давления).
Лучевые методы исследования, несомненно, имеют важное значение в диагностике ОСКН, а также в динамике для оценки эффективности консервативного лечения. Анамнестические, физикальные данные позволяют заподозрить причину острой кишечной непроходимости (перенесенные операции, характер, количество послеоперационных рубцов, периодические приступы болей, вздутия живота).
Исключительно важно установление у пациента наличия странгуляции, ишемии кишечника. КТ позволяет с высокой точностью выявить такие изменения. У 63 наших пациентов была заподозрена странгуляция, возможно, с развитием ишемии/некроза кишечника, перитонита. Для данной группы пациентов, характерными признаками были:
– тяжелое общее состояние: гипотония (признаки гиповолемического шока), САД < 75 мм рт. ст. (среднее артериальное давление), тахикардия (>100 в 1 мин.), по шкале ASA > 3 баллов;
– уровень лактата > 2,25 ± 0,18 м;
– гипокалиемия;
– по УЗИ органов брюшной полости — признаки синдрома кишечной недостаточности (СКН) 2–3 ст., свободная жидкость;
– при КТ: утолщение стенки кишки, при КТ с контрастированием — отсутствие или незначительные накопления контраста, симптом «мишени», газ в брыжеечных и воротной венах и выраженный отек/уплотнение брыжейки тонкой кишки;
– при выраженной гиповолемии изменения соответствуют так называемому «шоковому» кишечнику [16] и при КТ выявляются диффузная дилатация и утолщение стенок и складок тонкой кишки, усиленное накопление контраста в слизистой оболочке, скопление жидкости в просвете кишки;
– признаки гиповолемии (дегидратации) — повышение показателя гематокрита, уровня мочевины, креатинина.
Эти больные оперированы после предоперационной подготовки (стабилизация гемодинамики, коррекция электролитов, декомпрессия верхних отделов ЖКТ) открытым способом. Послеоперационная летальность в этой группе составила 6,3 % (n = 4), осложнения были у 12,69 % пациентов (парез, инфекции области хирургического вмешательства), средние сроки госпитализации составили 12,0 ± 1,7 дня. Средняя продолжительность оперативных вмешательств в среднем составила 118,0 ± 12,5 мин. Повторные операции до выписки из стационара потребовались 4 пациентам (6,3 %): по поводу ранней спаечной непроходимости (n = 2), несостоятельность ушитой перфорации или десерозированных участков кишки (n = 2).
При исследовании 197 пациентов с острой кишечной непроходимостью чувствительность обзорной рентгенографии живота составила 73 %, специфичность 53 %, а при КТ — 91 и 72 % соответственно, причем по рутинной рентгенографии невозможно судить о наличии странгуляции.
О наличии обструкции можно судить путем контрастирования тонкой кишки бария сульфатом или лучше водорастворимым контрастом (мы пользуемся урографином). Определение преимущества перед рутинной рентгенографией имеет УЗИ, в частности, и для исследования степени расширения кишечника при
ОСКН, и по данным литературы имеет чувствительность в 91 % и специфичность — 84 % [17].
Спаечный процесс в брюшной полости, как правило, развивается вследствие травмы париетальный/висцеральный брюшины после больших травматичных операций или в результате перитонита. Мы, по аналогии с классификацией перитонита академика В.Д. Федорова, по распространенности спаечный процесс оценили в 4 степени [18].
При спаечном процессе А степени выявляют, как правило, один послеоперационный рубец, чаще в правой подвздошной области при аппендэктомии, сбоку от него рубец на месте дренажа (по поводу местного перитонита) или в правом подреберье после холецистэктомии. При УЗИ, КТ, рентген-контрастном исследовании кишечника водорастворимым контрастом можно выявить единичную припаянную к передней брюшной стенке петлю кишечника.
При спаечном процессе В степени могут быть 2–3 послеоперационных рубца, включая после дренажей, при лучевых методах исследования — 1–3 припаянные петли кишечника. В анамнезе оперативные вмешательства по поводу деструктивных форм аппендицита, острого холецистита, острого осложненного дивертикулита ободочной кишки, осложненных диффузным перитонитом.
Для спаечного процесса С степени характерно наличие множественных рубцов по срединной линии, в боковых областях, после дренирования. При лучевых методах могут быть выявлены множественные петли, припаянные в различных областях живота, характерно наличие изолированных скоплений жидкости между раздутыми петлями кишечника. В анамнезе у больных оперативные вмешательства по поводу распространенного перитонита (перфорации полых органов, травмы полых органов) с релапаротомией, в т.ч. программированной санацией.
При спаечном процессе D степени у пациентов, как правило, рубец после срединной лапаротомии и/или другие рубцы, в т.ч. после множества дренажей. При лучевых методах исследования данные практически идентичны С степени. В анамнезе лапаротомии, релапаротомии, санационные лапаротомии или ведение по методике «открытого живота».
Результаты
По результатам до- и интраоперационного исследования А степень спаечного процесса была у 36 (37,14 %), В — у 21 (18,75 %), С — у 33 (29,46 %) и D степень — у 22 пациентов (19,64 %).
В целом общая летальность при ОСКН составила 2,03 %. 134 пациентам со стабильной гемодинамикой, без проявлений сепсиса и шока, планировали лапароскопию и, при возможности, лапароскопические вмешательства. В процессе диагностической лапароскопии условия для выполнения лапароскопического адгезиолизиса были установлены у 67 пациентов (46,2 %), в остальных случаях была конверсия на лапаротомию (табл. 1).
|
Причины конверсии |
Всего |
|
|
Абс. |
% |
|
|
Некроз кишки |
3 |
4,16 |
|
Перфорация кишки |
4 |
5,55 |
|
Десерозирование, требующее резекции |
1 |
1,38 |
|
Массивный спаечный процесс (конгломерат петель кишечника) |
15 |
20,83 |
|
Выраженный спаечный процесс, расширение петель кишечника, не позволяющие визуализировать причину, уровень непроходимости |
23 |
31,94 |
|
Необходимость интраоперационной декомпрессии |
8 |
11,11 |
|
Интраоперационная нестабильность гемодинамики |
18 |
18,35 |
Таблица 1. Причины и частота конверсии при лапароскопии
Table 1. Laparoscopy conversion causes and rates
Частота осложнений при лапароскопии составила 6,93 %, и они возникали при установлении первого троакара (2) или при попытке дальнейшей ревизии и рассечении спаек, данные осложнения также были показанием к конверсии. Основная часть причин конверсии к выполнению лапаротомии была обусловлена распространенными массивными, чаще висцеро-висцеральными спайками с формированием значительного конгломерата петель кишок, когда невозможно установить уровень препятствия, причинные спайки (52,77 %), причем в этой ситуации резко ограничено пространство для ревизии. У 4,16 % пациентов во время лапароскопии установлен некроз кишечника вследствие странгуляции, которая не была установлена до операции. При выявлении во время лапароскопии резко раздутой (>4 см), паретичной тонкой кишки возникает необходимость в декомпрессии, что технически крайне сложно выполнить (11,1 %).
Недооценка значения интраабдоминальной гипертензии в дооперационной гемодинамической нестабильности (гипотензия, снижение сатурации < 94 %) у 25 % пациентов и послужила причиной к экстренной лапаротомии. Исходная интраабдоминальная гипертензия (>12 мм рт. ст.) существенно усугубляется ввиду напряженного пневмоперитонеума, необходимого для лапароскопии, суммарно внутрибрюшное давление повышается > 24–25 мм рт. ст., что может соответствовать интраабдоминальной гипертензии III и иногда IV ст. [19][20]. Из 18 пациентов с подобным осложнением 14 были старше 60 лет с ХОБЛ или другой кардиореспираторной патологией.
Адгезиолизис проводили комбинированно-тупым и острым путем: при рыхлых, нежных брюшинных спайках эффективно и удобно тупое разделение, электрокоагуляцию применяли при шнуровидных васкуляризованных спайках, данный метод избегали при плотных, непосредственно припаянных друг к другу петлях кишечника (висцеро-висцеральные) или висцеропариетальных спайках, поскольку электрокоагуляция чревата перфорацией во время диссекции или на 3–5-е сутки послеоперационного периода.
Как известно, чаще всего осложнения лапароскопии связаны с первым этапом наложения пневмоперитонеума, которое выполняется вслепую. Относительная безопасность при распространенном спаечном процессе и резких раздутых петлях кишечника может быть достигнута способом «открытой» лапароскопии по Хассону, использованием иглы Вереша. Повреждение петли кишки нами отмечено в 2 случаях при использовании троакарного способа. 2 случая перфорации были связаны с диссекцией спаек при попытке освобождения петли кишки из спаечного конгломерата.
При спаечном процессе I ст. ОСКН первый троакар вводили в противоположной стороне от послеоперационного рубца (например, после аппендэктомии, параумбиликальный доступ или мезогастрии слева). Если в анамнезе операций более одной, не более 2–3 и в пределах одного этажа брюшной полости (II степень спаечного процесса), троакар вводили также в противоположной стороне от рубцов. Наиболее безопасно в таких случаях, а также при III степени спаечного процесса, выбирали точку в левом подреберье по среднеключичной линии или в левой подвздошной области (симметричные точки Мак-Бурнея).
Вообще при спаечных процессах 3–4-й степени чаще использовали способ открытой лапароскопии Хассона. Хотя, как было отмечено выше, при таких случаях предпочтение следует отдавать открытым операциям.
Необходимость в декомпрессии кишечника, по нашим данным, возникла у 11 % пациентов, окончательно показания к декомпрессии определяли после адгезиолизиса и при восстановлении перистальтики и цвета серозной оболочки кишечника и заполнении содержимым из раздутых отделов нижележащих от странгуляции петель, декомпрессию считали непоказанной.
Для профилактики рецидива спаечной кишечной непроходимости использовали «искусственный» пневмоперитонеум, для этого после освобождения брюшной полости от углекислого газа вводили кислород или воздух под внутрибрюшным давлением ≤ 12 мм рт. ст. Известно, что углекислый газ полностью элиминируется примерно через 45 мин, а кислород и воздух в течение 24 ч.
Частота конверсии также зависела от выраженности степени спаечного процесса и увеличивалась при более выраженном процессе (табл. 2).
|
Степень спаечного процесса |
Частота конверсии, % (n) |
Отношение рисков конверсии (ОР (95 % ДИ)) |
|
I степень |
8,33 (6) |
II/I ст.: 1,1667(0,4027–3,3803); р = 0,7764, z-критерий Фишера 0,284 |
|
II степень |
9,72 (7) |
III/I ст.: 4,1667 (1,7663–9,8293); р = 0,011, z-критерий Фишера 3,259 |
|
III степень |
34,72 (25) |
IV/I ст.: 5,6667 (2,4605–13,0504); р > 0,0001, z-критерий Фишера 4,75 |
|
IV степень |
47,22 (34) |
IV/III ст.: 1,3600 (0,8607–2,1490); р = 18,77, z-критерий Фишера 1,317 |
Таблица 2. Сравнительный анализ частоты конверсии от степени спаечного процесса
Table 2. Comparative analysis of conversion rate by grade of adhesions
Как следует из таблицы, риски конверсии при I и II степени спаечного процесса статистически не различаются, а при III степени риск конверсии по сравнению с I степенью до 9 раз, а при IV степени до 13 раз выше.
Сопоставление данных дооперационной диагностики и интраоперационной визуализации также подтверждает зависимость частоты конверсии от степени выраженности спаечного процесса, хотя было выявлено расхождение в оценке спаечного процесса (табл. 3). В частности, недооценка IV степени (27 случаев до- и 34 интраоперационно), гипердиагностика III степени (39 и 25 соответственно). Частота конверсии при дооперационной оценке I степени составила 13,95 % (у 6 из 43 пациентов), II степени — 28 % (у 7 из 25), III степени — 64,10 % (у 25 из 39 пациентов). Эти данные могут говорить о нецелесообразности попытки лапароскопии и лапароскопических оперативных вмешательств при спаечном процессе III и IV степени.
Из общего числа госпитализированных пациентов с ОСКН лапароскопические операции были выполнены в 31,47 %, и, по-видимому, уровень 31 % — пока адекватный прогностический показатель выполняемости лапароскопического адгезиолизиса при ОСКН. В то же время уровень выполняемости диагностической лапароскопии при дооперационной оценке распространенности спаечного процесса, тщательном выборе точки установки первого троакара может достичь 71 % (с учетом возможных осложнений, исходной интраабдоминальной гипертензии).
При ОСКН выполнение лапароскопической операции перед хирургом ставит следующие задачи (рис. 1).
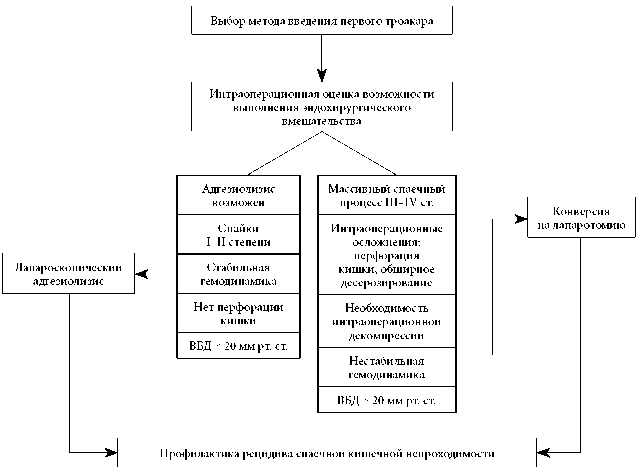
Рисунок 1. Основные задачи при оценке возможности лапароскопического вмешательства при ОСКН
Figure 1. Main procedures to assess laparoscopy feasibility in AASBO
Частота осложнений при выполнении диагностической лапароскопии составила 6,94 % (перфорация, десерозирование кишки).
После лапароскопического адгезиолизиса летальных случаев не было, осложнения в послеоперационном периоде были в 6,4 % (n = 4), парез (n = 2), инфекция области хирургического вмешательства (n = 1) (у 1 больного выполнена лапаротомия по поводу несостоятельности швов ушитой десерозированной кишки). Средние сроки госпитализации составили 6,5 ± 2,7 дня. Средняя продолжительность лапароскопических операций составила 75 ± 15 мин. Сравнительная оценка результатов открытых и лапароскопических операций приведена в таблице 3.
|
Показатели |
Частота |
Статистическая разница |
|
|
открытые операции |
лапароскопические операции |
||
|
Послеоперационные осложнения (%) |
12,69 |
6,4 |
ОР 1,968 (95 % ДИ: 0,624–6,20); р < 0,01 |
|
Послеоперационная летальность (%) |
6,3 |
0 |
р < 0,001 |
|
Средние сроки госпитализации (дни) |
12,0 ± 1,7 |
6,5 ± 2,7 |
р = 0,012 |
|
Средняя продолжительность операций (мин) |
118,0 ± 12,5 |
75,0 ± 25,0 |
р = 0,044 |
|
Повторные операции до выписки из стационара (%) |
6,3 |
1,6 |
ОР 3,936 (95 % ДИ: 0,452–34,240); р < 0,01 |
Таблица 3. Сравнительная оценка результатов открытых и лапароскопических операций
Table 3. Comparative assessment of open and laparoscopic surgery outcomes
Обсуждение
До недавнего времени основным методом хирургического лечения ОСКН была лапаротомия, а в последние годы распространены лапароскопические технологии, преимуществом которым являются уменьшение образования спаек, раннее восстановление функции кишечника, уменьшение послеоперационной боли, сроков пребывания в стационаре [21][22].
Кроме того, ЛСАЛ снижает риск осложнений, госпитальной смертности и хирургической инфекции [23].
В то же время в клинической практике ЛСАЛ используется только в 15 % случаев [22].
Необходимо подчеркнуть, что, несмотря на вышеперечисленные преимущества, они могут быть получены только при тщательном отборе пациентов с ОСКН, как правило, у наиболее легкого их контингента.
Как было нами показано, у тяжелых больных, с нестабильной гемодинамикой, перенесших более 2 операций по поводу ОСКН с проявлениями странгуляции, ишемии кишечника, интраабдоминальной гипертензии, показаны открытые оперативные вмешательства. При планировании лапароскопических операций у 134 пациентов с ОСКН они были возможны только у 46,2 %, у остальных (53,8 %) потребовалась конверсия на лапаротомию. Из общего числа больных с ОСКН ЛСАЛ был возможен у 31,47 %.
Как показало наше исследование, ЛСАЛ показан при спаечном процессе I–II степени, у больных со стабильной гемодинамикой, без тяжелой сопутствующей кардиореспираторной патологии и синдрома интраабдоминальной гипертензии. Преимуществами лапароскопических операций по сравнению с открытыми было снижение частоты послеоперационных осложнений (6,4 и 12,69 %) и летальности (6 и 6,3 %), сроков госпитализации (6,5 и 18 дней), необходимости в повторных операциях (1,6 и 6,3 %) и продолжительности операции (75 и 118 минут соответственно).
Заключение
При хирургическом лечении пациентов с ОСКН лапароскопические операции выполнимы, но при условии тщательного отбора больных. Важными показателями для определения выполнимости ЛСАЛ являются общее состояние, выраженность спаечного процесса, наличие странгуляции / выраженной ишемии кишечника, интраабдоминальной гипертензии, во время операции — необходимости декомпрессии кишечника, возникновения осложнений, нестабильности гемодинамики. Из общего числа пациентов с ОСКН лапароскопические операции были возможны в 31,47 % и, соответственно, показания к ЛСАЛ должны быть установлены на основании всесторонней оценки тяжести состояния пациентов и распространенности спаечного процесса.
Информация о конфликте интересов. Конфликт интересов отсутствует.
Информация о спонсорстве. Данная работа не финансировалась.
Список литературы
1. Norrbom C., Steding-Jessen M., Agger C.T., Osler M., Krabbe-Sorensen M., Settnes A., et al. Risk of adhesive bowel obstruction after abdominal surgery. A national cohort study of 665,423 Danish women. Am J Surg. 2019;217(4):694–703. DOI: 10.1016/j.amjsurg.2018.10.035
2. NELA Project Team. The second patient report of the National Emergency Laparotomy Audit (NELA). London: The Royal College of Anaesthetists; 2016.
3. Scott J.W., Olufajo O.A., Brat G.A., Rose J.A., Zogg C.K., Haider A.H., et al. Use of national burden to define operative emergency general surgery. JAMA Surg. 2016;151(6):e160480. DOI: 10.1001/jamasurg.2016.0480
4. Gale S.C., Shafi S., Dombrovskiy V.Y., Arumugam D., Crystal J.S. The public health burden of emergency general surgery in the United States: a 10-year analysis of the nationwide inpatient sample-2001 to 2010. J Trauma Acute Care Surg. 2014;77(2):202–8. DOI: 10.1097/TA.000000000000362
5. Samuel O., Olayide A., Ganiyu R., Funsho Y., Olusola A. Cost effectiveness analysis of duration of nonoperative management for adhesive bowel obstruction in a developing country. Malawi Med J. 2018;30(2):90–3. DOI: 10.4314/mmj.v30i2.7
6. Sakari T., Christersson M., Karlbom U. Mechanisms of adhesive small bowel obstruction and outcome of surgery; a population-based study. BMC Surg. 2020;20(1):62. DOI: 10.1186/s12893-020-00724-9
7. Krielen P., van den Beukel B.A., Stommel M.W., Van G.H., Strik C., Ten Broek R.P. In- hospital costs of an admission for adhesive small bowel obstruction. World J Emerg Surg. 2016;11:49. DOI:10.1186/s13017-016- 0109-9
8. Syrmis W., Richard R., Jenkins-Marsh S., Chia S.C., Good P. Oral water soluble contrast for malignant bowel obstruction. Cochrane Database Syst Rev. 2018;3(3):CD012014. DOI: 10.1002/14651858.CD012014.pub2
9. Ceresoli M., Coccolini F., Catena F., Montori G., Di Saverio S., Sartelli M., et al. Water-soluble contrast agent in adhesive small bowel obstruction: a systematic review and meta-analysis of diagnostic and therapeutic value. Am J Surg. 2016;211(6):1114–25. DOI: 10.1016/j.amjsurg.2015.06.012
10. Sallinen V., Di Saverio S., Haukijärvi E., Juusela R., Wikström H., Koivukangas V., et al. Laparoscopic versus open adhesiolysis for adhesive small bowel obstruction (LASSO): an international, multicentre, randomised, open-label trial. Lancet Gastroenterol Hepatol. 2019;4(4):278– 86. DOI: 10.1016/S2468-1253(19)30016-0
11. Quah G.S., Eslick G.D., Cox M.R. Laparoscopic versus open surgery for adhesional small bowel obstruction: a systematic review and metaanalysis of case-control studies. Surg Endosc. 2019;33(5):3209–17. DOI: 10.1007/s00464-018-6604-3
12. Zühlke H.V., Lorenz E.M.P., Straub E.M, Savvas V. Pathophysiology and classification adhesions. Langenbecks Arch Chir Suppl II Verh Dtsch Ges Chir. 1990:1009–16. PMID: 1983476
13. Coccolini F., Ansaloni L., Manfredi R., Campanati L., Poiasina E., Bertoli P., et al. Peritoneal adhesion index (PAI): proposal of a score for the “ignored iceberg” of medicine and surgery. World J Emerg Surg. 2013;8(1):6. DOI: 10.1186/1749-7922-8-6
14. Острая неопухолевая кишечная непроходимость у взрослых. Клинические рекомендации.. M.: Российское общество хирургов; 2016.
15. Kopitkó C., Medve L., Gondos T. The value of combined hemodynamic, respiratory and intra-abdominal pressure monitoring in predicting acute kidney injury after major intraabdominal surgeries. Ren Fail. 2019;41(1):150–8. DOI: 10.1080/0886022X.2019.1587467
16. Elst J., Ghijselings I.E., Zuidema W.P., Berger F.H. Signs of posttraumatic hypovolemia on abdominal CT and their clinical importance: A systematic review. Eur J Radiol. 2020;124:108800. DOI: 10.1016/j.ejrad.2019.108800
17. Jang T.B., Schindler D., Kaji A.H. Bedside ultrasonography for the detection of small bowel obstruction in the emergency department. Emery Med J. 2011;28(8);676–8.
18. Федоров Д.В. Лечение перитонита. M.: Медицина; 1974. 302 с.
19. Tayebi S., Gutierrez A., Mohout I., Smets E., Wise R., Stiens J., et al. A concise overview of non-invasive intra-abdominal pressure measurement techniques: from bench to bedside. J Clin Monit Comput. 2021;35(1):51–70. DOI: 10.1007/s10877-020-00561-4
20. De Waele J.J., Malbrain M.L., Kirkpatrick A.W. The abdominal compartment syndrome: evolving concepts and future directions. Crit Care. 2015;19:211. DOI: 10.1186/s13054-015-0879-8
21. Nordin A., Freedman J. Laparoscopic versus open surgical management of small bowel obstruction: an analysis of clinical outcomes. Surg Endosc. 2016;30(10):4454–63. DOI: 10.1007/s00464-016-4776-2
22. Hackenberg T., Mentula P., Leppaniemi A., Sallinen V. Laparoscopic versus open surgery for acute adhesive small-bowel obstruction: a propensity score-matched analysis. Scand J Surg. 2017;106(1):28–33. DOI: 10.1177/1457496916641341
23. Sajid M.S., Khawaja A.H., Sains P., Singh K.K., Baig M.K. A systematic review comparing laparoscopic vs open adhesiolysis in patients with adhesional small bowel obstruction. Am J Surg. 2016;212(1):138–50. DOI:10.1016/jamjsurg.2016.01.030
Об авторах
Ш. В. ТимербулатовРоссия
д.м.н., кафедра хирургии с курсом эндоскопии ИДПО,
Республика Башкортостан, Уфа
В. М. Сибаев
Россия
д.м.н., кафедра хирургии с курсом эндоскопии ИДПО,
Республика Башкортостан, Уфа
В. М. Тимербулатов
Россия
д.м.н., чл.-корр. РАН, профессор, кафедра хирургии с курсом эндоскопии ИДПО,
Республика Башкортостан, Уфа
М. В. Забелин
Россия
д.м.н., профессор, кафедра хирургии с курсом эндоскопии ИДПО,
Республика Башкортостан, Уфа
М. В. Тимербулатов
Россия
д.м.н., профессор, кафедра факультетской хирургии,
Республика Башкортостан, Уфа
Р. Б. Сагитов
Россия
д.м.н., кафедра хирургии с курсом эндоскопии ИДПО,
Республика Башкортостан, Уфа
А. Р. Гафарова
Россия
кафедра хирургии с курсом эндоскопии ИДПО,
Республика Башкортостан, Уфа
Рецензия
Для цитирования:
Тимербулатов Ш.В., Сибаев В.М., Тимербулатов В.М., Забелин М.В., Тимербулатов М.В., Сагитов Р.Б., Гафарова А.Р. Острая спаечная кишечная непроходимость: сравнительный анализ открытых и лапароскопических операций. Креативная хирургия и онкология. 2022;12(1):35-42. https://doi.org/10.24060/2076-3093-2022-12-1-35-42
For citation:
Timerbulatov Sh.V., Sibaev V.M., Timerbulatov V.M., Zabelin M.V., Timerbulatov M.V., Sagitov R.B., Gafarova A.R. Acute Adhesive Small Bowel Obstruction: a Comparative Analysis of Open and Laparoscopic Surgery. Creative surgery and oncology. 2022;12(1):35-42. (In Russ.) https://doi.org/10.24060/2076-3093-2022-12-1-35-42


































