Перейти к:
Роль микроокружения в распространении опухолей яичников
https://doi.org/10.24060/2076-3093-2021-11-4-278-283
Аннотация
Введение. Метастазы являются грозным осложнением злокачественных новообразований, и терапия распространенной формы заболевания в большинстве случаев неэффективна. Метастазирование — многоэтапный процесс, включающий в себя отделение раковой клетки от первичной опухоли, интравазацию, экстравазацию и инвазию опухолевой клетки в орган-мишень. Ранние этапы метастазирования хорошо изучены. Вопрос о том, как влияет микроокружение опухоли на прогрессирование и дальнейшее распространение заболевания, является дискуссионным.
Цель исследования: изучение адаптивных и реактивных свойств большого сальника при раке яичников с метастатическим поражением большого сальника на основе иммуногистохимического анализа.
Материалы и методы. Исследованы образцы тканей больших сальников 40 пациенток с верифицированным раком яичников III a и b стадий. В работе использовались методы световой микроскопии, материал фиксировали в 10 % растворе формалина, обезвоживали и заливали в парафин, окраска гематоксилином Майера и эозином. Иммуногистохимические методы исследования проводились с использованием моноклональных антител к белкам CD7, CD4, CD8, CD 68, VEGF, D2–40, CD44. Для статистической обработки данных использовали лицензионный пакет прикладных программ Statistica 7.0.
Результаты и обсуждение. В результате исследований тканей большого сальника обнаружено, что в некоторых случаях формируется лейкоцитарный вал вокруг метастатического очага. В составе лейкоцитарного вала определялось большее количество CD7+ и CD8+ клеток, что, возможно, влияло на сохранение реактивных и адаптивных свойств большого сальника. Также было выявлено увеличение клеток, экспрессирующих CD44 в тех образцах больших сальников, где отсутствовал лейкоцитарный вал. Количество клеток, экспрессирующих маркеры ангиогенеза, такие как VEGF, CD34, преобладало в тканях большого сальника без лейкоцитарного вала вокруг метастатического очага. Заключение. В тканях микроокружения опухоли могут происходить изменения, указывающие на сохранение или снижение адаптивных свойств органа, что способствует дальнейшему прогрессированию заболевания.
Ключевые слова
Для цитирования:
Халикова Л.В., Шевлюк Н.Н., Ганцев Ш.Х., Анварович Х.А., Хасанова И.Р. Роль микроокружения в распространении опухолей яичников. Креативная хирургия и онкология. 2021;11(4):278-283. https://doi.org/10.24060/2076-3093-2021-11-4-278-283
For citation:
Khalikova L.V., Shevlyuk N.N., Gantsev Sh.Kh., Khalikov A.A., Khasanova I.R. Role of Microenvironment in Ovarian Tumourisation. Creative surgery and oncology. 2021;11(4):278-283. (In Russ.) https://doi.org/10.24060/2076-3093-2021-11-4-278-283
Введение
Рак яичников является одним из онкологических заболеваний женской половой системы с высокими показателями смертности и характеризуется поздней выявляемостью. Около 70 % первично выявленного рака яичника составляют III и IV стадии. Эффективность терапии рака яичника на продвинутых стадиях остается крайне низкой, несмотря на достижения современной онкологии. Анти-PDL-терапия доказала свою эффективность против многих видов рака, однако при распространенном раке яичников результаты были очень скромными [1][2]. Метастатический процесс включает в себя инициацию, отделение раковой клетки, интравазацию, экстравазацию и колонизацию в органе мишени. Основным местом локализации метастазов при раке яичников является большой сальник. Он регулирует перитонеальный гомеостаз [3]. Опухолевые клетки рака яичников, оказавшиеся в перитонеальной полости, имплантируются на поверхность большого сальника. Инвазия опухолевых клеток и прогрессия метастазирования тесно связаны со взаимодействием раковых клеток и опухолевого микроокружения [4–6]. Большой сальник, учитывая его клеточный состав, должен обладать противоопухолевым иммунитетом, однако в некоторых случаях опухолевые клетки могут трансформировать клетки большого сальника в свое микроокружение [7][8]. И механизм патогенеза этой трансформации нуждается в уточнении [9]. При этом до сих пор неизвестно, каким образом клетки микроокружения опухоли участвуют в дальнейшем прогрессировании метастазирования. Более глубокое изучение изменений микроокружения опухоли и метастатических очагов поможет в поиске новых механизмов иммуносупрессии и новых мишеней для таргетной терапии этого грозного заболевания.
Целью нашего исследования явилось изучение адаптивных и реактивных свойств большого сальника при раке яичников с метастатическим поражением большого сальника на основе иммуногистохимического анализа.
Материалы и методы
Материалом исследований явился большой сальник пациенток, полученный во время операций по поводу рака яичников IIIa стадии (n = 40) в Республиканском клиническом онкологическом диспансере г. Уфы. Гистологический тип опухоли во всех исследуемых группах — низкодифференцированная аденокарцинома. Возраст пациенток находился в пределах от 50 до 67 лет. Материал фиксировали в 10 % растворе формалина, обезвоживали в спиртах возрастающей концентрации и заливали в парафин. Гистологические срезы окрашивали гематоксилином Майера и эозином. Для иммуногистохимического исследования использовали моноклональные антитела к белкам CD7, CD4, CD8, CD68, VEGF, D2–40 CD34, CD44, E-cad, CD61 (табл. 1).
Таблица 1. Мышиные моноклональные антитела для иммуногистохимического исследования
Table 1. Murine monoclonal antibodies used in immunohistochemistry
|
Антиген (краткая характеристика) |
Клон; разведение; производитель |
|
CD 4 — маркер Т-хелперов |
1F6; 1: 15 Diagnostic BioSystems, США |
|
CD 7 — маркер Т-клеток |
CBC.37; 1:10; Diagnostic BioSystems, США |
|
CD 8 — маркер цитотоксических Т-лимфоцитов |
144B; 1:50; Diagnostic BioSystems, США |
|
CD 44 — интегральный клеточный гликопротеин, играющий важную роль в межклеточных взаимодействиях, клеточной адгезии и миграции |
156–3 С11; 1:50; Diagnostic BioSystems, США |
|
CD 34 — мембранный белок, молекула клеточной адгезии, маркер эндотелиоцитов кровеносных сосудов |
QBEND/10; 1:50; Diagnostic BioSystems, США |
|
CD 61 — мембранный белок из семейства интегринов |
Y2/51; 1:100; Diagnostic BioSystems, США |
|
D240 — маркер к эндотелиоцитам лимфатических сосудов |
D2–40; 1:100; Dako, Дания |
|
CD 68 — маркер макрофагов |
Kp-1; 1:20; Cell Marque, США |
|
VEGF — фактор роста сосудов |
VG1; 1:10; Diagnostic BioSystems, США |
|
E-cadherin |
36; 1:20; BioGenex, Нидерланды |
При разведении антител использовали разбавитель Antibody Diluent (SPRING Bioscience, США). Система детекции — Reveal Polyvalent HRP — DAB Detection System (SPRING Bioscience, США). Окраска проводилась ручным и аппаратным способом с использованием автостейнера Ventana xt.
Морфометрию структур большого сальника проводили на условной единице площади. На препаратах, окрашенных иммуногистохимическими методами, определяли количество позитивно окрашенных клеток. Для статистической обработки данных использовали лицензионный пакет прикладных программ Statistica 7.0 (Stat Soft Inc., США). Анализ соответствия вида распределения количественных признаков по закону нормальности проводили с помощью критерия Шапиро — Уилка. Сравнительный анализ групп проводился с помощью параметрических (критерий Стьюдента) и непараметрических методов (U-критерий Манна — Уитни). Различия считали статистически значимыми при p < 0,05. Для выполнения работы было получено добровольное информированное согласие пациенток на участие в проведенном исследовании. На выполнение работы имеется разрешение локального этического комитета Оренбургского государственного медицинского университета (протокол заседания локального этического комитета № 237 от 16 октября 2019 года).
Результаты и их обсуждение
В результате проведенного исследования было отмечено, что в 66 % случаев в большом сальнике пациенток формировался лейкоцитарный вал вокруг метастатического очага (рис. 1).
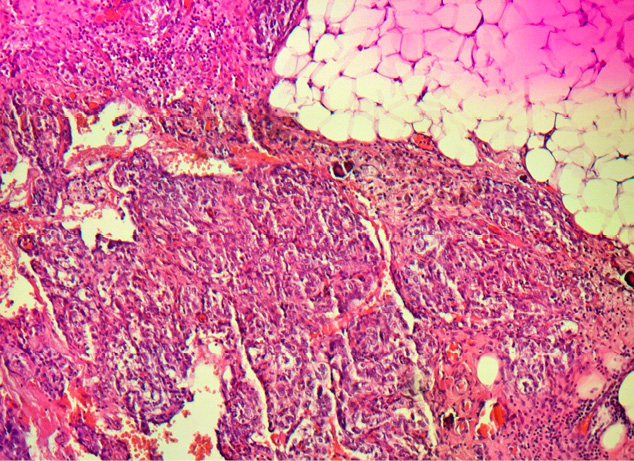
Рисунок 1. Лейкоцитарный вал вокруг метастатического очага большого сальника.
Окраска гематоксилин-эозин Майэра. Увеличение ×100
Figure 1. Leucocyte-bank metastatic focus encapsulation in greater omentum.
Mayer’s haematoxylin and eosin, 100×
Выживаемость пациенток с наличием лейкоцитарного вала оказалась выше, чем у пациенток без вала вокруг метастатического очага (р < 0,05). При выполнении иммуногистохимического исследования с применением моноклональных антител было обнаружено, что количество клеток, экспрессирующих СD8, было значительно выше (р < 0,01) у пациенток первой группы, у них в большом сальнике выявлялся лейкоцитарный вал вокруг метастатического очага. Число клеток, окрашенных позитивно маркером CD7, было статистически значимо выше в первой группе (p < 0,02). По числу клеток позитивных в отношении маркеров макрофагов CD68 и лимфоцитов хелперов CD4 статистически значимых различий не выявлено (табл. 2).
Таблица 2. Содержание CD8+, CD7+ клеток в больших сальниках с лейкоцитарным валом вокруг метастатического очага и без лейкоцитарного вала
Table 2. CD8+ and CD7+ cell counts in greater omentum samples with and without leucocyte-bank encapsulation of metastatic foci
|
Маркеры |
Большой сальник с лейкоцитарным валом вокруг метастатического очага |
Большой сальник без лейкоцитарного вала вокруг метастатического очага |
р |
|
Мe (Q1–Q3) |
Мe (Q1–Q3) |
||
|
CD8 |
89,5 (77,0–100,0) |
47,0 (43,0–54,0) |
0,01* |
|
CD4 |
10,5 (7,0–11,0) |
10,0 (6,0–20,0) |
0,88 |
Снижение содержания клеток лимфоидного ряда, таких как CD8, CD7, в окружении метастатического очага способствует опухолевому росту и приводит к прогрессированию заболевания. Количество тканевых макрофагов CD68 сохраняется при опухолевом росте, но при нарушении в работе Т-лимфоцитов, возможно, не влияет на выживаемость.
При анализе результатов, полученных путем иммуногистохимического выявления клеток, экспрессирующих маркеры ангио-, лимфангиогенеза, было выявлено, что число клеток, положительно окрашенных VEGF, выше в образцах большого сальника без лейкоцитарного вала вокруг метастатического очага (p < 0,05). Также количество клеток, экспрессирующих D2–40 и СD34, было статистически значимо ниже в образцах тканей большого сальника с лейкоцитарным валом вокруг метастатического очага. Это согласуется с концепцией неоангиогенеза и лимфангиогенеза, стимулируемых опухолевыми клетками для их собственного роста и прогрессирования заболевания.
Из исследованных молекул адгезии статистически значимы различия по количеству клеток, экспрессирующих CD44 (p < 0,02). Число позитивно окрашенных клеток выше в образцах большого сальника без лейкоцитарного вала вокруг метастатического очага.
Метастазирование — это не автономный процесс и в значительной степени зависит от тканевого микроокружения. Взаимодействие между раковыми клетками, иммунными клетками, эндотелиальными клетками может приводить к прогрессированию злокачественного роста. В литературе имеются данные, что опухолевые клетки выделяют молочную кислоту (продукт анаэробного гликолиза), участвующую в сигнальных путях, индуцирующих ангиогенез, путем экспрессии сосудистого эндотелиального фактора VEGF. Вместе с тем молочная кислота может влиять на усиление экспрессии аргиназы-1 опухоль-ассоциированными макрофагами, тем самым приводя их в активное состояние [10]. Также в литературе имеются данные исследований, показывающие, что опухоль-ассоциированные макрофаги CD68 при злокачественных новообразованиях органов головы и шеи не являются прогностически значимыми и не влияют на выживаемость по сравнению с макрофагами CD163 [11]. Рак яичников сопровождается системной иммуносупрессией, однако пациенты с хорошим иммунным ответом имеют более высокие показатели выживаемости и демонстрируют хороший ответ на химиотерапию. В иммунном ответе участвуют Т-лимфоциты, экспрессирующие CD8 и CD4 на поверхности клеток. CD8+ — это цитотоксические лимфоциты, уничтожающие чужеродные антигены при помощи специфических ферментов перфорина и гранзима В. CD4+ клетки способны рекрутировать и активировать другие клетки, такие как макрофаги, В-лимфоциты, дендритные и иные [12].
Наличие CD8+ лимфоцитов коррелирует с хорошей выживаемостью [13][14]. Результаты наших исследований подтверждают, что ткани большого сальника, пораженного метастазами, в составе которого повышается количество СD8+, СD7+ клеток, сохраняют свои реактивные свойства и могут задерживать прогрессию опухолевого роста. Также увеличение количества клеток, экспрессирующих маркеры ангио- и лимфангиогенеза, на фоне уменьшения количества клеток, экспрессирующих CD8+ и CD7+, может указывать на снижение адаптивных свойств большого сальника, приводящих к распространению опухолевого процесса.
Увеличение количества СD44+ клеток в образцах большого сальника без лейкоцитарного вала вокруг метастатического очага может указывать на снижение реактивных свойств большого сальника, что приводит к имплантации большего числа опухолевых клеток на мезотелии большого сальника. Имеются исследования, доказывающие, что интегральный гликопротеид CD44, экспрессируемый на поверхности опухолевой клетки, способствует прикреплению ее к поверхности мезотелия путем секретирования матриксных металлопротеаз. Выраженная экспрессия данного белка коррелирует с плохим прогнозом [15].
Заключение
В нашем исследовании выявлено, что в 66 % случаев формировался лейкоцитарный вал вокруг метастатического очага. Формирование лейкоцитарного вала вокруг метастатического очага большого сальника может указывать на сохранение его адаптогенных и реактивных свойств, которые проявляются повышением количества CD8+ и CD7+ клеток, снижением количества клеток, экспрессирующих маркеры ангиогенеза и молекулы адгезии клетки CD44. Нарушение в работе клеток Т-лимфоидного ряда и макрофагов в условиях опухолевого роста приводит к изменению микроокружения метастатического очага большого сальника, что может способствовать развитию ангио- и лимфангиогенеза и дальнейшему снижению защитных свойств большого сальника.
Информация о конфликте интересов. Конфликт интересов отсутствует.
Информация о спонсорстве. Данная работа не финансировалась.
Список литературы
1. Westergaard M.C.W., Milne K., Pedersen M., Hasselager T., Olsen L.R., Anglesio M.S., et al. Changes in the tumor immune microenvironment during disease progression in patients with ovarian cancer. Cancers (Basel). 2020;12(12):3828. DOI: 10.3390/cancers12123828
2. Blanc-Durand F., Genestie C., Galende E.Y., Gouy S., Morice P., Pautier P., et al. Distribution of novel immune-checkpoint targets in ovarian cancer tumor microenvironment: a dynamic landscape. Gynecol Oncol. 2021;160(1):279–84. DOI: 10.1016/j. ygyno.2020.09.045
3. Krishnan V., Tallapragada S., Schaar B., Kamat K., Chanana A.M., Zhang Y., et al. Omental macrophages secrete chemokine ligands that promote ovarian cancer colonization of the omentum via CCR1. Commun Biol. 2020;3(1):524. DOI: 10.1038/s42003-020-01246-z
4. Tahmasebi Birgani M., Carloni V. Tumor microenvironment, a paradigm in hepatocellular carcinoma progression and therapy. Int J Mol Sci. 2017;18(2):405. DOI: 10.3390/ijms18020405
5. Friedl P., Alexander S. Cancer invasion and the microenvironment: plasticity and reciprocity. Cell. 2011;147:992–1009. DOI: 10.1016/j. cell.2011.11.016
6. Бриллиант Ю.М., Бриллиант А.А., Сазонов С.В. Эпителиальные кадгерины и ассоциированные с ними молекулы при инвазивном дольковом раке молочной железы. Архив патологии. 2017;79(1):12–8. DOI: 10.17116/patol201779112-18
7. Cao L., Hu X., Zhang Y., Sun X.T. Omental milky spots in screening gastric cancer stem cells. Neoplasma. 2011;58(1):20–6. DOI: 10.4149/ neo_2011_01_20
8. Auer K., Bachmayr-Heyda A., Sukhbaatar N., Aust S., Schmetterer K.G., Meier S.M., et al. Role of the immune system in the peritoneal tumor spread of high grade serous ovarian cancer. Oncotarget. 2016;7(38):61336–54. DOI: 10.18632/oncotarget.11038
9. Liu J., Geng X., Li Y. Milky spots: omental functional units and hotbeds for peritoneal cancer metastasis. Tumour Biol. 2016;37(5):5715–26. DOI: 10.1007/s13277-016-4887-3
10. Colegio O.R., Chu N.Q., Szabo A.L., Chu T., Rhebergen A.M., Jairam V., et al. Functional polarization of tumour-associated macrophages by tumour-derived lactic acid. Nature. 2014;513(7519):559–63. DOI: 10.1038/nature13490
11. Troiano G., Caponio V.C.A., Adipietro I., Tepedino M., Santoro R., Laino L., et al. Prognostic signifi cance of CD68+ and CD163+ tumor associated macrophages in head and neck squamous cell carcinoma: a systematic review and meta-analysis. Oral Oncol. 2019;93:66–75. DOI: 10.1016/j.oraloncology.2019.04.019
12. Turner T.B., Buchsbaum D.J., Straughn J.M., Randall T.D., Arend R.C. Ovarian cancer and the immune system — the role of targeted therapies. Gynecol Oncol. 2016;142(2):349–56. DOI: 10.1016/j. ygyno.2016.05.007
13. Santoiemma P.P., Reyes C., Wang L.P., McLane M.W., Feldman M.D., Tanyi J.L., et al. Systematic evaluation of multiple immune markers reveals prognostic factors in ovarian cancer. Gynecol Oncol. 2016;143(1):120–7. DOI: 10.1016/j.ygyno.2016.07.105
14. Sato E., Olson S.H., Ahn J., Bundy B., Nishikawa H., Qian F., et al. Intraepithelial CD8+ tumor-infi ltrating lymphocytes and a high CD8+/ regulatory T cell ratio are associated with favorable prognosis in ovarian cancer. Proc Natl Acad Sci U S A. 2005;102(51):18538–43. DOI: 10.1073/pnas.0509182102
15. Nakamura K., Sawada K., Kinose Y., Yoshimura A., Toda A., Nakatsuka E., et al. Exosomes promote ovarian cancer cell invasion through transfer of CD44 to peritoneal mesothelial cells. Mol Cancer Res. 2017;15(1):78–92. DOI: 10.1158/1541-7786.MCR-16-0191
Об авторах
Л. В. ХаликоваРоссия
Халикова Лариса Вячеславовна, кафедра гистологии
Республика Башкортостан, Уфа
Н. Н. Шевлюк
Россия
Шевлюк Николай Николаевич — д.б.н., профессор, кафедра гистологии, цитологии и эмбриологии
Оренбург
Ш. Х. Ганцев
Россия
Ганцев Шамиль Ханафиевич, д.м.н., профессор, кафедра онкологии с курсами онкологии и патологической анатомии ИДПО
Республика Башкортостан, Уфа
Х. А. Анварович
Россия
Халиков Айрат Анварович, д.м.н., профессор, кафедра судебной медицины
Республика Башкортостан, Уфа
И. Р. Хасанова
Россия
Хасанова Ильмира Раисовна, кафедра гистологии
Республика Башкортостан, Уфа
Рецензия
Для цитирования:
Халикова Л.В., Шевлюк Н.Н., Ганцев Ш.Х., Анварович Х.А., Хасанова И.Р. Роль микроокружения в распространении опухолей яичников. Креативная хирургия и онкология. 2021;11(4):278-283. https://doi.org/10.24060/2076-3093-2021-11-4-278-283
For citation:
Khalikova L.V., Shevlyuk N.N., Gantsev Sh.Kh., Khalikov A.A., Khasanova I.R. Role of Microenvironment in Ovarian Tumourisation. Creative surgery and oncology. 2021;11(4):278-283. (In Russ.) https://doi.org/10.24060/2076-3093-2021-11-4-278-283
JATS XML


































