«Креативная хирургия и онкология» («Creative surgery and oncology») - рецензируемый научно-практический журнал открытого доступа.
Издается с 2009 года, перерегистрирован Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) 29 мая 2017 года (Свидетельство о регистрации ПИ № ФС 77-69907 от 29.05.2017 - печатное издание).
Зарегистрирован в качестве средства массовой информации с формой распространения «сетевое издание» Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) 19 февраля 2020 года (Регистрационный номер ЭЛ № ФС 77-77899 от 19.02.2020 - сетевое издание).
Учредитель: Федеральное государственное бюджетное образовательное учреждение высшего образования «Башкирский государственный медицинский университет» Министерства здравоохранения Российской Федерации
Периодичность: 4 выпуска в год.
Языки: русский, английский
Территория распространения - Российская Федерация, зарубежные страны
В журнале публикуются передовые статьи о новых направлениях научных исследований в области хирургии и онкологии, а также новых методах лечения и диагностики.
Журнал ориентирован на практических врачей хирургических специальностей, научных работников и студентов, преподавателей медицинских учебных заведений, организаторов здравоохранения, а также тех, кто проявляет интерес к достижениям современной медицины.
Текущий выпуск
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Введение. Меланома кожи — агрессивная злокачественная опухоль нейроэктодермального происхождения. Согласно статистике большинство пациентов начинают лечение на 2-й и 3-й стадиях заболевания. Это усугубляет прогноз и определяет необходимость расширения объема хирургического лечения. Цель исследования: улучшить исходы операций на лимфатическом аппарате у пациентов с меланомой кожи. Материалы и методы. Проведен анализ 190 историй болезней пациентов с меланомой кожи. Путем статистического анализа оценена целесообразность эскалации и деэскалации вмешательств. В группе пациентов с 3-й стадией сформирована проспективная выборка из 43 человек, у которых операции проводились с использованием интраоперационных методик профилактики лимфореи. Результаты и обсуждение. Лимфаденэктомия с профилактической целью не оптимальна в связи с тем, что бóльшая часть пациентов не имеет признаков поражения лимфатических узлов на момент операции. Отказ от проведения расширенного вмешательства не всегда отвечает требованиям онкологической безопасности. Из 43 пациентов с метастатическим поражением лимфатических узлов имели поражение только 1 лимфатического узла 25 человек, 2 и более лимфатических узлов — 18 человек. При отказе от лимфаденэктомии высокий риск рецидива возможен у 41 % пациентов. У пациентов с 1-й стадией меланомы кожи отмечен низкий процент поражения лимфоколлекторов, как и регионарного метастазирования в отдаленном периоде. У пациентов с 3-й стадией заболевания возрастает вероятность послеоперационных нежелательных явлений. Пломбировка лимфатических сосудов, бережное отношение к окружающим структурам и использование оптического увеличения показывают хорошие результаты в профилактике послеоперационной лимфореи, что влечет снижение риска других осложнений. Заключение. Выбор типа оперативного вмешательства у пациентов с меланомой кожи должен быть обусловлен анализом прогнозов, взвешен в соответствии с возможными рисками и, при необходимости, дополнен применением средств профилактики осложнений.
Введение. Пациенты с морбидным ожирением (ИМТ ≥ 35 кг/м²) являются группой высокого риска развития послеоперационных вентральных грыж из-за повышенного внутрибрюшного давления, особенностей анатомии и сопутствующих заболеваний. Основной причиной формирования грыж являются послеоперационные осложнения (серомы, гематомы, нагноения, эвентрации), а также факторы, повышающие внутрибрюшное давление (кашель, запоры, физические нагрузки и др.). Цель исследования: снижение частоты образования послеоперационных вентральных грыж и послеоперационных осложнений у пациентов с морбидным ожирением. Материалы и методы. Разработанный и внедренный в клиническую практику способ профилактики образования послеоперационных вентральных грыж у пациентов высокого риска, который заключается в превентивном протезировании лапаротомного доступа. Способ заключается в установке синтетического импланта (полипропилена) в ретромускулярное пространство с фиксацией к апоневрозу внутренних косых мышц живота. Результаты. Техническим результатом использования способа является формирование плотного соединительнотканного рубца и снижение частоты образования послеоперационных вентральных грыж за счет минимизации риска миграции и отторжения синтетического импланта. Обсуждение. Согласно приведенным данным статистически значимо (p = 0,039) снизилась частота образования послеоперационных вентральных грыж в сравниваемых группах с 30,7 до 5,2 %. Различия в развитие сером и гематом в основной и контрольной группах статистически не значимы (>0,05) и составили 21,05 и 19,2 %, которые разрешились самостоятельно без инвазивных вмешательств. Заключение. Пациентам с морбидным ожирением с целью снижения риска образования послеоперационных вентральных грыж рекомендовано выполнение превентивного протезирования при проведении оперативных вмешательств лапаротомным доступом. Преимущество в использовании способа заключается в уменьшении послеоперационных осложнений, в том числе возникновения хронического болевого синдрома, и улучшении качества жизни пациентов.
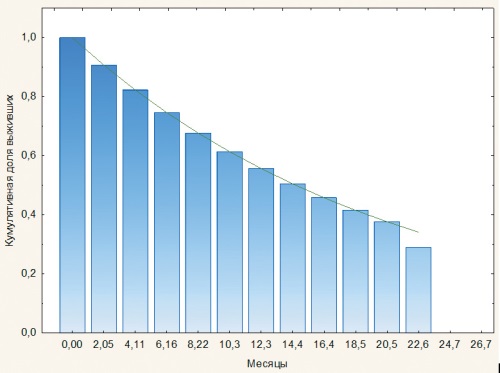
Введение. Гепатоцеллюлярная карцинома занимает третье место среди причин смертности от рака в мире с крайне низкой пятилетней выживаемостью (20,3 %), а метастазы колоректального рака в печень составляют значительные 10–20 % всех вторичных опухолей. Трансартериальная химиоэмболизация (ТАХЭ) является стандартным методом локального паллиативного лечения, однако после процедуры формируется устойчивая гипоксическая среда, способствующая агрессивным рецидивам и дальнейшему прогрессированию заболевания. Цель исследования: оценить клиническую эффективность и безопасность ТАХЭ у пациентов с первичным и метастатическим раком печени. Материал и методы. Проведен ретроспективный анализ 333 пациентов (181 мужчина, 152 женщины) в возрасте от 19 до 83 лет (средний возраст 60,1 ± 0,55 года), пролеченных в ФГБУ «НМИЦ онкологии» МЗ РФ. У 93 пациентов была диагностирована гепатоцеллюлярная карцинома (МКБ-10 C22.0), у 240 — метастазы колоректального рака в печень (МКБ-10 C78.7). Всем выполнена процедура ТАХЭ. Двухлетнюю выживаемость анализировали с помощью таблиц дожития, метода Каплана — Мейера и регрессионного анализа Кокса для изучения факторов риска. Статистический анализ выполнен в программе Statistica 10. Результаты и обсуждение. За два года наблюдения умерли 61,9 % пациентов, общая выживаемость составила 38,1 %. Наибольший риск смерти отмечался в первые два месяца после ТАХЭ, оставаясь высоким до восьмого месяца. Анализ по Каплану — Мейеру показал значительное снижение выживаемости после пяти месяцев. Факторами риска были стадия заболевания, морфология опухоли и пол пациента: метастатическое поражение и мужской пол ассоциировались с более низкой выживаемостью. Заключение. Общая выживаемость после ТАХЭ остается низкой, особенно в первые месяцы. Выявленные факторы риска позволяют точнее определять группы высокого риска для оптимизации комплексной терапии и разработки более эффективных стратегий лечения.
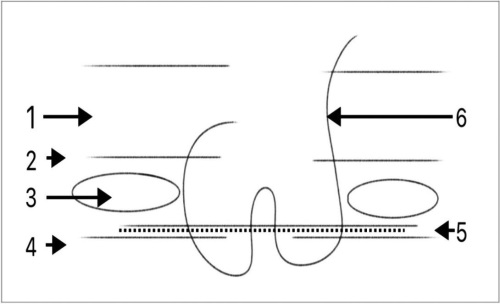
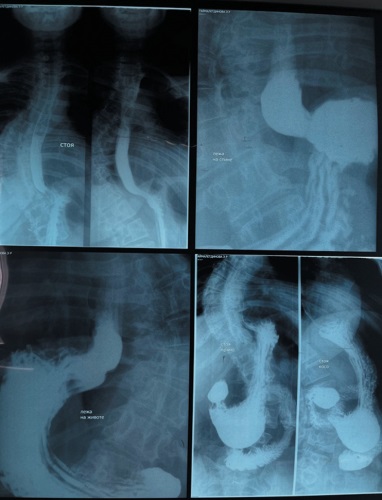
Введение. Грыжа пищеводного отверстия диафрагмы (ГПОД) — это заболевание, при котором происходит ослабление связочного аппарата диафрагмы, в следствие чего происходит растяжение и увеличение пищеводного отверстия диафрагмы, что приводит к выходу органов брюшной полости в плевральную полость. Распространенным методом хирургического лечения ГПОД является лапароскопическая фундопликация по Ниссену с дальнейшем выполнением до или после передней или задней крурорафией. Альтернативным методом является применение робот-ассистированной хирургии. Материалы и методы. С апреля 2022 года по январь 2024 года в торакальном хирургическом отделении Клиники БГМУ выполнено 113 робот-ассистированных лапароскопических фундопликаций. Пациенты были разделены на две группы: Исследовательская группа (n=65): выполнена робот-ассистированная лапароскопическая фундопликация по Ниссену с модифицированной крурорафией и фиксацией манжеты Z-образными швами по патенту № 2813330C1. Контрольная группа (n=48): выполнена стандартная лапароскопическая фундопликация по Ниссену с передней крурорафией узловыми швами. Все оперативные вмешательства выполнены на роботической системы Da Vinci Si. Результаты и обсуждение. Применение патента № 2813330C1 при робот-ассистированных вмешательствах при ГПОД 3 степени предотвращает миграцию манжеты, в том числе и в плевральную полость, соскальзывание и возникновение симптома «телескопа». Позволяет предотвратить деформацию, достичь симметричности и предотвратить соскальзывание манжеты, а также обеспечивает раннюю активацию пациентов и начало энтерального питания за счет использования лапароскопической техники и Z-образного шва нерассасывающимся шовным материалом. Заключение. Проведенные нами оперативные вмешательства при ГПОД 3 степени с применением патента № 2813330C1 и положительные результаты позволяют рассчитывать на то, что предлагаемый нами способ найдет широкое применение в видеоэндоскопической хирургии.
Введение. Внедрение принципов ERAS-протокола (Esophagectomy Complications Consensus Group) в торакальную хирургию требует обеспечения раннего энтерального питания, в том числе после резекции пищевода по Льюису. Однако высокая частота несостоятельности пищеводно-желудочного анастомоза и послеоперационной энцефалопатии препятствует безопасному применению сиппингового питания, что требует совершенствования методов профилактики этих осложнений. Цель исследования. Оценить эффективность внедренных способов профилактики несостоятельности пищеводно-желудочного анастомоза и энцефалопатии при резекции пищевода по Льюису. Материалы и методы. Проведен ретроспективно-проспективный анализ результатов лечения 121 пациента с резекцией пищевода по Льюису. В основной группе (n = 35) применены способы профилактики несостоятельности пищеводно-желудочного анастомоза и послеоперационной энцефалопатии, защищенные патентами РФ № 2791399 C1 и № 2810178 C1. Контрольную группу (n = 86) составили пациенты, оперированные по стандартной методике. Результаты. Применение предложенных способов в основной группе обеспечило стойкое снижение случаев несостоятельности анастомоза (0 % против 4,7 %, p < 0,05), статистически значимое снижение общей частоты послеоперационных осложнений (8,6 % против 17,4 %, p < 0,05), госпитальной летальности (2,9 % против 12,8 %, p < 0,05) и длительности госпитализации (16 ± 3 против 21 ± 4 суток, p < 0,05). В основной группе не зарегистрированы признаки послеоперационной энцефалопатии, нарушения сознания, когнитивных функций и лабораторных показателей, ассоциированных с гипераммониемией. Обсуждение.Полученные данные подтверждают, что предложенные способы профилактики направлены на ключевые патогенетические механизмы формирования осложнений: несостоятельности анастомоза и энцефалопатии, ассоциированной с портальной гипертензией. Устранение билиарной гипертензии и интраоперационный контроль герметичности анастомоза позволяют безопасно реализовать сиппинговое питание и способствуют сокращению сроков реабилитации. Заключение. Применение предложенных способов профилактики несостоятельности анастомоза и послеоперационной энцефалопатии при резекции пищевода по Льюису позволяет обеспечить герметичность швов, избежать метаболических и когнитивных нарушений в раннем послеоперационном периоде и безопасно реализовать сиппинговое питание. Полученные результаты, пусть и не основанные на большом массиве наблюдений, подтверждают патогенетическую обоснованность подхода и обосновывают перспективы его дальнейшего клинического применения.
Введение. Одномоментная реконструкция молочной железы с использованием гладких круглых имплантатов вновь приобрела актуальность после отказа от текстурированных моделей из-за ассоциации с BIA-ALCL. Однако отдаленные результаты DTI-реконструкции с гладкими имплантами остаются слабоизученными. Настоящее исследование направлено на оценку безопасности и эффективности этого метода. Материалы и методы. В ретроспективное исследование включены 48 пациенток (64 молочные железы), перенесших подкожную мастэктомию с одномоментной реконструкцией гладкими имплантатами (без использования дополнительных укрывающих материалов). Период наблюдения составил в среднем 54,5 месяца. Проанализированы частота осложнений, онкологические и хирургические данные, а также факторы риска удаления или замены имплантатов. Результаты. Ранние осложнения составили 10,94 % (наиболее частое — частичный некроз ареолы), поздние — 20,31 % (преимущественно капсулярная контрактура III–IV ст. по Бейкеру). В 75 % случаев имплантат был сохранен. Высокий ИМТ, большой объем имплантата и вес удаленной ткани были значимыми факторами в развитии осложнений. Обсуждение. Полученные данные демонстрируют сопоставимые или лучшие показатели по сравнению с зарубежными исследованиями. Отсутствие укрывающих материалов и субпекторальная установка не увеличивали частоту инфекций, но коррелировали с анимационной деформацией. Наличие послеоперационной лучевой терапии существенно повышало риск контрактуры. Заключение. Одномоментная реконструкция молочной железы с применением гладких имплантатов демонстрирует удовлетворительные отдаленные результаты при низком уровне осложнений. Метод может рассматриваться как безопасная альтернатива в условиях ограниченного доступа к ADM.
Введение. Аддитивное производство керамики на основе гидроксиапатита (ГА) рассматривается как перспективный подход к созданию персонализированных костных имплантатов, однако высоконагруженные фотополимерные суспензии требуют точного подбора состава и режимов засветки для обеспечения стабильной печати и качества изделий. Целью работы явилась разработка фотополимерной суспензии на основе гидроксиапатита собственного синтеза для аддитивного производства керамических имплантатов методом DLP-3D-печати. Материалы и методы. Гидроксиапатит синтезировали методами соосаждения и гидротермального синтеза из водных растворов солей кальция и фосфатов, проводили помол и фракционирование порошка, морфологию оценивали с помощью сканирующей электронной микроскопии, элементный состав — методом энергодисперсионного рентгенофлюоресцентного анализа. На основе синтезированного гидроксиапатита была разработана фотополимерная суспензия с массовой долей неорганической фазы 60 %, содержащая акрилатные мономеры, фотоинициирующую систему и диспергирующие добавки. Также исследовали фотополимеризацию на DLP-3D-принтере при различной мощности ультрафиолетового излучения и времени экспозиции. Результаты и обсуждение. Было показано формирование хорошо кристаллизованного гидроксиапатита с пластинчатой и наноструктурированной морфологией и развитой пористостью, подтверждено преобладание кальция и фосфора без значимых токсичных примесей. При мощности излучения 40 мВт/см² оптимальное время экспозиции 6–10 с обеспечивало формирование равномерно отвержденных слоев толщиной около 0,7–0,9 мм и выход на плато по толщине при дальнейшем увеличении выдержки. Заключение. Полученные данные свидетельствуют, что сочетание контролируемой морфологии гидроксиапатита и специально подобранной фотополимерной матрицы обеспечивает достаточную глубину полимеризации и стабильность слоев, необходимых для DLP-печати изделий сложной геометрии. Высокая удельная поверхность и пористость ГА дополнительно повышают его потенциал в тканевой инженерии. Разработанная фотополимерная суспензия на основе ГА собственного синтеза демонстрирует пригодность для DLP-3D-печати и может быть использована как основа для создания персонализированных керамических имплантатов в травматологии, ортопедии, нейрохирургии и челюстнолицевой хирургии.
КЛИНИЧЕСКИЙ СЛУЧАЙ
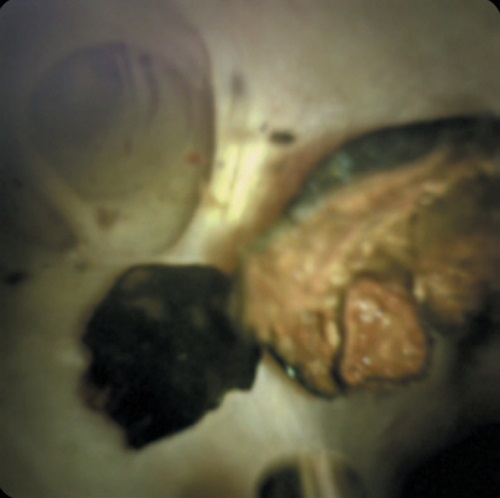
Введение. Трансплантация печени является окончательным методом лечения для пациентов с поражениями печени терминальных стадий. У реципиентов трансплантированной печени способны возникать стриктуры билиодигестивного анастомоза, холелитиаз различной локализации. У ряда пациентов со сложными формами холелитиаза и билиарных стриктур применение рутинной эндоскопической процедуры может оказаться неэффективным. В подобных ситуациях перспективен метод прямой цифровой холангиоскопии SpyGlass DS™. Материалы и методы. Клинический случай: у пациента 66 лет в позднем послеоперационном периоде после ортотопической родственной трансплантации печени диагностированы стриктура реконструктивного гепатикоеюноанастомоза на петле по Ру и внутрипеченочный холелитиаз. Произведено гибридное вмешательство — баллонная дилатация стриктуры и внутрипеченочная литотрипсия, литоэкстракция с использованием холангиоскопии SpyGlass DS™, а также чрескожное чреспеченочное дренирование желчевыводящих путей под контролем рентгенографической системы. Результаты и обсуждение. Выполнение прямой холангиоскопии позволило безопасно устранить гепатолитиаз и стриктуру гепатикоеюноанастомоза у пациента после трансплантации печени. Выполнение наружного дренирования с возможностью отсроченной холангиографии позволило контролировать функцию желчевыделения и поэтапно производить замену дренажей. Заключение. Прямая цифровая холангиоскопия выступает важным инструментом диагностики и лечения билиарных осложнений у реципиентов трансплантированной печени.
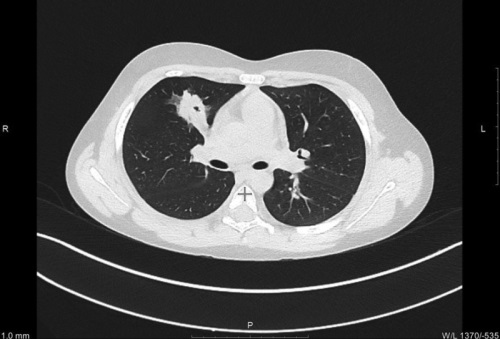
Введение. Рак легкого у детей — крайне редкая патология, встречающаяся менее чем в 0,2 % случаев всех детских опухолей. Наиболее часто выявляются аденокарцинома и карциноидные опухоли, которые, как показывают последние мультицентровые исследования, нередко диагностируются уже на поздних стадиях из-за отсутствия специфической симптоматики и трудностей дифференциальной диагностики. Материалы и методы. В статье представлен клинический случай инвазивной муцинозной аденокарциномы легкого у ребенка 9 лет. Результаты. Опухоль выявлена случайно при выполнении компьютерной томографии грудной клетки. Изменения в легких были расценены как деструктивная пневмония, по поводу которой пациент длительно получал лечение, на фоне которого наступило клиническое улучшение. Однако при контрольной компьютерной томографии была выявлена отрицательная динамика. Учитывая локализацию изменений в одной доле, после проведенной предоперационной подготовки пациенту была выполнена верхняя лобэктомия с систематической медиастинальной лимфодиссекцией. Гистологически установлен диагноз: инвазивная муцинозная аденокарцинома легкого. Специальное противоопухолевое лечение не проводилось. Пациент находится под динамическим наблюдением без признаков рецидива. Обсуждение. Данный клинический случай показывает проблемы диагностики рака легкого у детей, а также проблемы стадирования заболевания и определения тактики лечения. Заключение. Подчеркивается необходимость разработки четких клинических рекомендаций по диагностике и лечению рака легкого у детей с учетом анатомо-физиологических особенностей детского организма.
ОБЗОР ЛИТЕРАТУРЫ
В обзоре представлен анализ современной научной литературы, посвященной острой неокклюзионной мезентериальной ишемии (ОНМИ) — тяжелейшей патологии с летальностью до 80 %. Рассматриваются ключевые аспекты патогенеза, основные факторы риска и особенности клинической картины, затрудняющие раннюю диагностику. Особое внимание уделено возможностям и ограничениям современных методов диагностики, включая мультиспиральную компьютерно-томографическую ангиографию (МСКТ-А) и определение биомаркеров. Подробно проанализированы стратегии консервативного лечения (антикоагулянтная, системная вазодилатационная терапия) и хирургических вмешательств, включая реваскуляризацию, резекцию нежизнеспособных участков кишки и тактику damage control surgery. Обсуждается критически важная роль эксплоративной лапаротомии и лапароскопии в верификации диагноза и интраоперационной оценки жизнеспособности кишечника. Подчеркивается необходимость мультидисциплинарного подхода и создания специализированных центров для улучшения исходов лечения.
Послеоперационные осложнения являются насущной проблемой клинической медицины, ухудшая прогноз и повышая риск летального исхода у хирургических пациентов, особенно в абдоминальной и онкологической хирургии. Согласно современным представлениям микроциркуляторная дисфункция является важным патофизиологическим фактором, лежащим в основе гипоперфузии тканей и развития неблагоприятных послеоперационных исходов. В данном обзоре обобщены современные данные о взаимосвязи между нарушениями микроциркуляции (в области операции и в организме в целом) и послеоперационными осложнениями в абдоминальной хирургии. В обзоре рассматриваются следующие вопросы: (1) эпидемиология послеоперационных осложнений и актуальность этой проблемы в клинической хирургии и реаниматологии; (2) патофизиология периоперационных микроциркуляторных нарушений, включая геморрагический шок, диссеминированное внутрисосудистое свертывание (ДВС-синдром) и эндотелиальную дисфункцию; (3) органоспецифические изменения микроциркуляции при хирургических заболеваниях; (4) современные методы диагностики и мониторинга для оценки тканевой перфузии; (5) прогностическое и диагностическое значение ряда параметров микроциркуляции; и (6) современные терапевтические подходы к оптимизации тканевой перфузии и профилактике осложнений. Понимание важной роли микроциркуляции в обеспечении перфузии и оксигенации тканей обосновывает применение методов интенсивной терапии, ориентированных на микроциркуляцию и, следовательно, предупреждение ишемии органов и риска инфекционных и других послеоперационных осложнений.
Минимизация риска развития послеоперационных осложнений напрямую зависит от уровня биосовместимости имплантационных систем, что в наибольшей степени определяется состоянием и свойствами их поверхности. Покрытия на основе гидроксиапатита (ГАП) характеризуются структурно-функциональными особенностями, максимально приближенными к характеристикам костной ткани, что обусловливает их широкое применение в биомедицинской инженерии. Следовательно, нанесение гидроксиапатита в качестве модифицирующего покрытия поверхности способно существенно повысить биосовместимость имплантатов и активировать процессы остеоинтеграции. На сегодняшний день формирование тонких покрытий ГАП преимущественно осуществляется методами термического напыления, реализуемыми при температурах, близких к температуре плавления исходного материала. Однако воздействие высоких температур приводит к снижению биосовместимости конечного покрытия и ограничивает возможность введения в его состав термолабильных биоактивных добавок. В связи с этим технологии холодного напыления представляют собой перспективное направление, потенциально превосходящее классические термические методы. Тем не менее высокая хрупкость гидроксиапатита существенно осложняет получение прочных и равномерных покрытий при низкотемпературной обработке. Таким образом, выбор оптимального технологического подхода и установление рациональных параметров напыления являются ключевыми условиями формирования покрытий, обладающих требуемыми физико-химическими характеристиками, обеспечивающими повышение эффективности остеоинтеграции. В настоящей работе представлен систематический анализ экспериментальных исследований, направленных на разработку концептуальных основ подбора параметров порошка, подложки и холодного газодинамического напыления, ориентированных на получение высококачественных гидроксиапатитовых покрытий с улучшенными биомедицинскими свойствами.
Объявления
2020-12-25
Журнал «Креативная хирургия и онкология» включён в перечень изданий, рецензируемых ВАК
Приказом Министерства науки и высшего образования Российской Федерации от 9.12.2020 г. № 427-р «О включении в перечень, рецензируемых научных изданий, в которых должны быть опубликованы основные научные результаты диссертаций на соискание ученой степени кандидата наук, на соискание ученой степени доктора наук» журнал «Креативная хирургия и онкология» включён в перечень изданий, рецензируемых ВАК.
| Еще объявления... |
ISSN 2307-0501 (Online)