ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Введение. Торакальная эпидуральная анестезия/анальгезия (ТЭАА) и опиоидная внутривенная мультимодальная анальгезия (ММА) позволяют адекватно контролировать периоперационную боль, но сравнительные данные отсутствуют. Целью исследования было сравнить оба метода анестезии по стрессовому ответу во время и после робот-ассистированной тазовой эвисцерации (РАТЭ). Материалы и методы. Сто двенадцать пациентов были поровну разделены на 2 группы. Сывороточный кортизол определяли при индукции анестезии и 2, 24, 48 часов спустя. Эффективность анальгезии сравнивали с помощью 10-балльной числовой шкалы боли. Потребление обезболивающих средств и побочные эффекты были зарегистрированы в течение 1–3 дней после операции. Результаты. Уровень кортизола увеличился через 2 часа после разреза кожи в группе ММА и только через 24 часа в группе ТЭАА (р < 0,050). Послеоперационный уровень кортизола был значительно ниже в группе ТЭАА (р = 0,001). Числовые оценки болевого синдрома были значительно меньше в группе ТЭАА (1,7 [1,0–3,2] против 2,7 [2,1–4,2]; 1,9 [1,0–3,3] против 3,5 [3,5–5,0]; 3,7 [3,0–4,8] против 4,2 [3,7–4,7] соответственно; р < 0,050). Пациентам группы ТЭАА вводили меньше опиоидов (4,3 против 13,9 мг; 7,0 против 19,9 мг; 10,9 против 16,5 мг соответственно; р < 0,050). Не было существенной разницы в частоте дыхательной депрессии между двумя группами пациентов. Обсуждение. Результаты нашего исследования показали, что периоперационная реакция на стресс была снижена при добавлении ТЭАА к протоколу анестезии. Пациенты группы ТЭАА получили меньшие дозы анальгетиков. Аналогичные краткосрочные послеоперационные результаты были отмечены в обеих группах. Заключение. По сравнению с опиоидной ММА ТЭАА обеспечивала лучшую анальгезию и аналогичные профили побочных эффектов и представляется приемлемым методом подавления стрессового ответа и обезболивания у пациентов, перенесших РАТЭ.
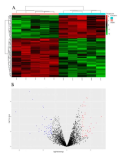
Введение. Рак шейки матки (РШМ) остается наиболее распространенным раком у женщин во всем мире, и до сих пор для диагностики и прогнозирования РШМ отсутствуют эффективные и специфические биомаркеры. В последние годы большое внимание привлекло изучение потенциала циркулярных РНК (циркРНК) как новых диагностических, прогностических и терапевтических инструментов. В текущем исследовании мы провели углубленное биоинформатическое исследование по изучению регуляторной сети «циркРНК — микроРНК (миРНК)- матричной РНК (мРНК)», чтобы выявить важные молекулярные процессы и биологические пути, предположительно связанные с РШМ. Материалы и методы. В ходе исследования были собраны данные об экспрессии циркРНК (GSE102686), миРНК (GSE30656) и мРНК генов-мишеней (GSE9750), основанные на базе данных «Омнибус экспрессии генов» (англ. Gene Expression Omnibus, или GEO), в образцах плоскоклеточного рака шейки матки и нормального плоского эпителия шейки матки, разделив их на исследуемую и контрольную группы. Для более глубокого понимания функции циркРНК для их генов-мишеней был проведен анализ белок-белкового взаимодействия (PPI), Генной онтологии (GO — Gene Ontology) и анализ Киотской энциклопедии генов и геномов (KEGG). Результаты. В отношении РШМ было выявлено в общей сложности 105 дифференциально экспрессируемых циркулярных РНК (ДЭЦ), 144 дифференциально экспрессируемых микроРНК (ДЭМ) и 539 дифференциально экспрессируемых генов-мишеней (ДЭГ). Одновременно анализ функционального обогащения GO и путей KEGG проводился для ДЭГ. Впоследствии благодаря базам данных по поиску циркРНК, миРНК и мРНК генов-мишеней, а также сетевому анализу PPI и функциональному обогащению мы обнаружили 3 ДЭЦ со значительно более высоким уровнем экспрессии (hsa_circ_0000745, hsa_circ_0084927 и hsa_circ_0002762), 6 ДЭМ с пониженным уровнем экспрессии (hsa-miR-145, hsa-miR-876-3p, hsa-miR-1229, hsa-miR-182, hsa-miR520h и hsa-miR-1252) и 9 ключевых генов, таких как ANGPT2, COL11A1, MEST, KIF20A, CLN6, FNDC3B, USP18, DLGAP5 и CXCL9, что позволяет предположить их потенциально значительную роль при РШМ. Заключение. Понимание регуляторной сети «циркРНК — миРНК — мРНК» имеет большое значение в понимании онкогенеза РШМ, а также обнаружении новых циркРНК как главных регуляторных молекул в данной сети — это новое направление в диагностике и таргетной терапии РШМ.
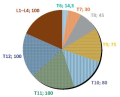
Введение. Выбор метода лечения между экстракраниальной стереотаксической лучевой терапией и хирургией метастатической опухоли тела позвонка с минимальным эпидуральным распространением или без эпидуральной компрессии твердой мозговой оболочки в настоящее время четко не определен. Материалы и методы. В исследование включен 41 пациент, получивший лечение в ФГБУ «НМИЦ онкологии» Минздрава России с 01.01.2014 по 31.12.2022. Критерием включения в исследование явилось наличие метастатической опухоли позвонка при условии отсутствия или с наличием минимальной эпидуральной компрессии твердой мозговой оболочки и области корешковой воронки (ESCC 0–1b). Больные были разделены на две группы: 21 пациент (группа SBRT) получил только экстракраниальную стереотаксическую лучевую терапию и 20 больных, которым проведено хирургическое вмешательство с последующей адъювантной экстракраниальной стереотаксической лучевой терапией через 1 месяц после операции (Oр. + Аd.SBRT). Результаты. В раннем послеоперационном периоде в группе SBRT не отмечалось ухудшения неврологического статуса больных, не отмечено улучшения функционального состояния по шкале Карновского и регресса болевого синдрома в отличие от больных группы Oр. + Аd.SBRT. Продолженный рост в группе SBRT возник у 3 (21%) пациентов, в группе Oр. + Аd.SBRT — только у 1 пациента (6%) через 1 месяц после операции. Обсуждение. В группе Oр. + Аd.SBRT в раннем послеоперационном периоде отмечалось улучшение функционального статуса, регресс болевого синдрома носил значимо более выраженный характер, чем у больных группы SBRT, что можно объяснить прямой декомпрессией сдавленного спинномозгового корешка и ликвидацией нарастающей нестабильности позвоночного столба. Заключение. У пациентов с метастатическим поражением позвоночника с минимальным эпидуральным распространением без эпидуральной компрессии спинного мозга при выраженном болевом синдроме и признаках нарастающей нестабильности позвоночного столба хирургическое лечение, дополненное адъювантной экстракраниальной стереотаксической лучевой терапией, является предпочтительным методом лечения.
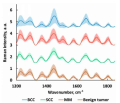
Введение. В последние десятилетия мы наблюдаем значительный рост заболеваемости раком кожи. Целью нашей работы является совершенствование специализированной техники и улучшение качества диагностики новообразований кожи. Материалы и методы. Основным методом исследования, который мы использовали в работе, был способ неинвазивной дифференциальной диагностики новообразований кожи, основанный на оптических методах исследования, в том числе метод спектроскопии комбинационного рассеяния, рамановской спектроскопии. Около 10 лет кафедрой онкологии на базе Самарского областного клинического онкологического диспансера (СОКОД) проводилось исследование, в которое вошли более полутысячи наблюдений. Для исследования были взяты образцы различных новообразований кожи, полученные при хирургическом лечении пациентов. При проведении экспериментальных испытаний получали определенный спектр, характеризующий различные доброкачественные и злокачественные образования кожи человека, в том числе меланому. Результаты. Результатом серии экспериментальных испытаний стало создание экспериментальной установки, абсолютно безопасной в применении. Обсуждение. Необходимо отметить, что важным является факт использования сопоставления индивидуальных характеристик спектра КР, которые получены при исследовании новообразования и здоровой кожи, для каждого пациента, что позволяет индивидуализировать метод. Высокий показатель точности 92% (с чувствительностью 89%, специфичностью 93%) очень важен для организации массового обследования, поскольку практически исключено возникновение ложных отрицательных результатов. Заключение. Принципиальная схема предложенного прибора не нуждается в использовании расходных материалов и различных реактивов, что понижает временные затраты и техническую трудоемкость при использовании способа. Метод рамановской спектроскопии новообразований кожи имеет возможность стать повсеместным и использоваться в лечебно-профилактических учреждениях любого профиля.
Введение. Новая коронавирусная инфекция COVID-19 оказала негативное влияние на хирургическую службу. Клинические рекомендации лечения хирургических пациентов адаптировались к новым условиям эпидемиологического неблагополучия с переориентацией на ургентную мини-инвазивную хирургическую помощь. Поэтому общепринятые позиции из лечебно-диагностического алгоритма не могли применяться из-за массового поступления пациентов в крайне тяжелом состоянии. К таким позициям относится проблема лечения и профилактики интраабдоминальной гипертензии и абдоминального компартмент-синдрома. Цель исследования: провести анализ результатов лечения пациентов с инфекцией COVID-19 в ковидных госпиталях, осложненной абдоминальной хирургической патологией и ассоциированной с абдоминальным хирургическим заболеванием, с позиции диагностики, лечения и профилактики патологических состояний, приводящих к повышению внутрибрюшного давления. Материал и методы. Проведен анализ результатов лечения 1900 пациентов с COVID-19 в ковид-госпиталях с разными хирургическими возможностями, где им были проведены диагностические и лечебно-профилактические мероприятия в отношении профилактики абдоминального компартмент-синдрома, т.е. использовался лечебно-диагностический алгоритм управления интраабдоминальной гипертензией и абдоминальным компартмент-синдромом. Результаты и обсуждение. В клинической группе у 67 (3,5 %) пациентов развилось абдоминальное хирургическое осложнение или ковид-инфекция ассоциировалась с острым абдоминальным хирургическим заболеванием. При наличии показаний к экстренной операции хирургическая тактика заключалась в использовании мини-инвазивных технологий и регионарной анестезии, при развитии компартмент-синдрома выполнялась экстренная декомпрессионная лапаротомия. Заключение. Использование лечебно-диагностического алгоритма управления интраабдоминальной гипертензией и абдоминальным компартмент-синдромом в клинической группе пациентов с COVID-19 позволило у 3,5 % пациентов провести профилактику компартмент-синдрома, а при ее развитии выполнить раннюю декомпрессионную лапаротомию у 1,5 % пациентов. Летальность от абдоминальных осложнений COID-19 в клинической группе составила 1,3 %.
Введение. Глиобластома — злокачественная нейроэпителиальная опухоль головного мозга с агрессивным течением и неблагоприятным прогнозом. Медиана общей выживаемости составляет 14,6 месяца. Высокая частота рецидивов за счет большой скорости репопуляции опухолевых клонов, невозможность радикального удаления первичной опухоли объясняют сравнительно небольшую эффективность стандартных методов лечения. Одним из способов усиления локального контроля при глиомах является симультанный интегрированный буст. Материалы и методы. В ходе исследования проанализированы данные 25 пациентов, получивших химиолучевое лечение по поводу глиобластомы Grade 4 в Радиотерапевтическом отделении № 1 с сентября 2021 по март 2023 года (данные проанализированы в течение 1 года). В первой группе 15 пациентов получали лучевую терапию с симультанным интегрированным бустом (SIB-VMAT) в рамках химиолучевого лечения. Во второй группе 10 пациентов получали лучевую терапию в стандартном режиме фракционирования. Результаты и обсуждение. Переносимость лечения была удовлетворительной: целевая доза подведена у 100% больных без необходимости в вынужденных перерывах, показатели токсичности сопоставимы в обеих группах; 1-летний локорегионарный контроль составил в группе с применением симультанного интегрированного буста 46,7%, в группе стандартного режима фракционирования — 50%; 1-летняя общая выживаемость в группе с применением симультанного интегрированного буста составила 66,7%, в группе стандартного режима — 70%. В течение срока наблюдения случаев радионекроза зафиксировано не было. Результаты, полученные авторами в ходе настоящего исследования, сопоставимы с данными актуальных научных публикаций по теме исследования. Заключение. Лучевая терапия с использованием симультанного интегрированного буста в послеоперационном лечении глиобластомы Grade 4 — приемлемый и безопасный метод с умеренной токсичностью и удовлетворительными показателями общей выживаемости.
Введение. Саркопения определяется как клинический синдромом, характеризующийся прогрессивным заболеванием скелетных мышц, с потерей мышечной массы и силы, что приводит к ухудшению физической работоспособности. Распространенность саркопении в популяции варьирует от 5 до 13% среди людей в возрасте 43,0 ± 11,1 года и достигает 50% среди лиц старше 70 лет. Для диагностики саркопении используются различные методы, которые, однако, имеют свои ограничения, и на данный момент компьютерная томография считается наиболее точным методом для определения саркопении. В связи с этим актуальна разработка новых методов ранней диагностики саркопении. Цель нашего исследования заключается в изучении различных методов диагностики саркопении у пациентов, страдающих от морбидного ожирения. Материалы и методы. Авторами представлен анализ различных методов диагностики саркопении у больных морбидным ожирением, в том числе запатентованным способом, основанным на исследованиях, проведенных в клинике БГМУ на базе ФГБОУ ВО МЗ РФ (патент на изобретение № 2815157 от 11.03.2024). Результаты и обсуждение. При использовании предложенного способа диагностики саркопении, значении индекса саркопении, равному или меньшему 15, врачи диагностировали наличие саркопении. Заключение. Распространенность и степень тяжести саркопении сильно варьируют в зависимости от используемых классификационных критериев и пороговых значений. С учетом отсутствия единого метода диагностики необходимо не только продолжение исследований этой проблемы, но и внедрение в широкую клиническую практику подходов, направленных на активное выявление, профилактику и коррекцию саркопении. Показатели саркопении и ожирения, полученные при дополнительном предоперационном исследовании, предоставляют значимую прогностическую информацию, превосходящую индекс массы тела, и помогут определить направления и объем оперативных вмешательств, направленных на улучшение результатов выживаемости.
ОБЗОР ЛИТЕРАТУРЫ
Метастазы являются ключевым механизмом распространения злокачественных опухолей, при котором клетки опухоли отделяются от первичного очага и формируют новые опухолевые узлы в различных частях организма. Костная ткань, включая позвоночник, часто поражается метастазами, что может значительно ухудшить прогноз и качество жизни пациентов. Метастазирование представляет собой сложный многоэтапный процесс, в ходе которого клетки опухоли претерпевают молекулярные и фенотипические изменения, позволяющие им мигрировать и адаптироваться к новым условиям в организме. Костные метастазы могут быть остеолитическими, вызывающими разрушение костей, или остеобластными, стимулирующими избыточное формирование костной ткани. Опухолевые клетки, попадая в кость, активируют остеокласты или остеобласты, что приводит к перестройке костной ткани и образованию замкнутого цикла разрушения костей и роста опухоли. Особенности опухолевых клеток определяются их генетическими и эпигенетическими изменениями, а также взаимодействием с окружающей средой. Понимание молекулярных и патофизиологических аспектов метастазирования в позвоночнике играет ключевую роль в разработке эффективных методов лечения и улучшении подходов к терапии. В данной работе рассматриваются новые терапевтические подходы, направленные на преодоление метастазирования в позвоночник с целью улучшения прогноза и качества жизни пациентов.
Интраабдоминальная гипертензия и абдоминальный компартмент-синдром остаются сложной проблемой абдоминальной хирургии. Ввиду разнообразных этиологических факторов, ведущих к повышению интраабдоминального давления (воспалительные, деструктивные процессы, травмы, сепсис, послеоперационные осложнения и др.), отрицательного влияния повышенного ИАД на функции гастроинтестинальной, дыхательной, сердечно-сосудистой систем, почек, центральную нервную систему, своевременная диагностика и лечение играют важную роль. Постепенно повышенное внутрибрюшное давление может вызвать стойкую дисфункцию органов и быть потенциально фатальным. На сегодня достаточно глубоко изучены патофизиологические механизмы, методы определения интраабдоминального давления, частоты его измерения, методы консервативного и хирургического лечения. В статье представлен обзор литературы по проблеме внутрибрюшной гипертензии и абдоминального компартмент-синдрома. Рассматриваются вопросы эпидемиологии, показатели летальности, методы измерения внутрибрюшного давления, в том числе современные инновационные технологии. Представлены основы клинической диагностики, значение и информативность дополнительных биохимических исследований крови, лучевых методов, преимущественно компьютерной томографии, ультразвукового исследования. Рассмотрены современные методы консервативного лечения, которые при раннем их применении существенно минимизируют повреждение органов-мишеней, органную дисфункцию, показания к экстренной декомпрессивной лапаротомии. Приведены также рекомендации по послеоперационному ведению пациентов с «открытым» животом, по оптимальным срокам закрытия лапаростомы.
Онкологические заболевания являются второй причиной смертности в Российской Федерации. Продление жизни пациентов с онкологической патологией предусматривает лечение токсическими препаратами с множественными побочными явлениями. Сегодня ученые всего мира стремятся найти препараты без токсических явлений. Мы обратились к фитостеролам. Фитостеролы — это класс стероидов, широко распространенных в растениях как важный компонент мембран растительных клеток. К ним относятся стигмастерол, бета-ситостерол, кампестерол. При раке печени было найдено, что стигмастерол повышает экспрессию проапоптотических генов (Bax, p53) и снижает экспрессию антиапоптотического гена Bcl-2 в клетках рака печени HepG2. Стигмастерол способен вызывать остановку клеток в фазе G0-G1 (стационарная фаза), в результате чего в фазе G2/M (фаза деления) оказывается намного меньше клеток. Стигмастерол индуцирует апоптоз и защитную аутофагию в клетках рака желудка, ингибируя при этом сигнальный путь Akt/mTOR. β-ситостерол проявляет ингибирующее рост и цитотоксическое действие против ряда установленных линий раковых клеток in vitro и in vivo, но не вызывает острых/подострых токсических эффектов. β-ситостерол широко используется для лечения хронических заболеваний предстательной железы. В США за 2020 год потребители с этой целью потратили 24 827 065 долларов на биологически активные добавки, содержащие бета-ситостерол. Кампестерол индуцирует апоптоз клеток через митохондриальный путь. Кампестерол цитотоксичен по отношению к клеткам U937 гепатоцеллюлярного рака. Кампестерол вызывает апоптоз клеток и активирует проапоптотические сигналы в клеточных линиях рака яичников человека. В данном обзоре литературы мы убедительно показали, что конкретные вещества этой группы — бета-ситостерол, стигмастерол и кампестерол — обладают выраженным противоопухолевым эффектом.
КЛИНИЧЕСКИЙ СЛУЧАЙ
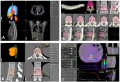
Введение. Перитонеальный канцероматоз, являющийся одной из наиболее агрессивных форм метастазирования, представляет собой серьезную клиническую проблему. Традиционные методы лечения, такие как циторедуктивная хирургия и системная химиотерапия, ограничены в своей эффективности. Новые подходы, включающие фотодинамическую терапию и флуоресцентную диагностику, открывают перспективные направления для улучшения результатов комплексного лечения данной категории больных. Материалы и методы. В статье представлен клинический случай лечения пациентки с перитонеальными метастазами рака яичника, осложненного нарушением тонкокишечной проходимости и некрозом опухоли, демонстрирующий результаты комплексного применения фотодинамических технологий и этапного циторедуктивного хирургического лечения. На первом этапе циторедуктивного оперативного вмешательства, приоритетной целью которого являлось устранение жизнеугрожающих осложнений, выполнялись флуоресцентная диагностика и фотодинамическая терапия для контроля полноты циторедукции, оценки характера подозрительных опухолевых очагов и воздействия на резидуальную опухоль. В рамках второго этапа хирургического лечения осуществлялись завершение циторедукции под контролем флуоресцентной диагностики и внутрибрюшная химиогипертермическая перфузия. Также проведена оценка результатов применения флуоресцентной диагностики для определения опухолевого поражения брюшины в целях объективизации выбора объема перитонэктомии. Результаты и обсуждение. Применение описанного подхода за счет интраоперационной диагностики и направленного противоопухолевого воздействия на остаточные опухолевые очаги привело к повышению эффективности циторедуктивного вмешательства. Оценка качества жизни по анкете SF-36 в послеоперационном периоде продемонстрировала значимое улучшение как физического, так и психологического компонентов здоровья в течение трех месяцев наблюдения. Заключение. Интеграция фототераностики в программу циторедуктивного оперативного лечения больных перитонеальным канцероматозом представляет собой инновационный подход, который обладает потенциальной возможностью повышения не только точности интраоперационной диагностики распространенности опухолевого процесса по брюшине, но и эффективности циторедуктивных вмешательств. Однако для полной оценки лечебного потенциала и подтверждения эффективности предложенного варианта лечения требуются дальнейшие клинические исследования.
Введение. Внеорганные кисты забрюшинного пространства (ВКЗП) были и остаются сложной проблемой в контексте определения тактики диагностики и лечения. В большинстве случаев ВКЗП протекают бессимптомно, что объясняет их выявляемость как случайную находку во время исследований или хирургических вмешательств на брюшной полости и/или забрюшинном пространстве по поводу других заболеваний. Основным методом лечения истинных и сформированных ложных ВКЗП является хирургический, который осуществляется как из лапаротомного, так и из лапароскопического доступов. Материалы и методы. Клинический случай: пациентка М., 39 лет, обратилась в поликлинику по месту жительства с жалобами на периодические боли внизу живота, в левом боку. По результатам исследований был выставлен диагноз «опухоль левого яичника больших размеров, осложненная болевым синдромом». Сопутствующий диагноз: многоузловая миома матки. Планировалось оперативное лечение лапаротомным доступом из-за больших размеров новообразования — консервативная миомэктомия. Интраоперационно, в левой подвздошной области забрюшинно обнаружено объемное жидкостное образование размерами 20×15 см, не связанное с яичником. Пациентка после дообследования направлена в плановом порядке на оперативное лечение по поводу забрюшинного образования в ГКБ № 21. Результаты и обсуждение. Операция была выполнена лапароскопическим способом. Продолжительность хирургического вмешательства составила 39 минут. Послеоперационный период протекал без осложнений. Дренажи удалены на вторые сутки. Пациентка выписана на 5-е сутки после операции. При гистологическом исследовании стенки кисты эпителиальная выстилка не была выявлена, стенка состояла из фиброзной ткани. В данном клиническом случае, согласно результатам гистологического исследования, строение стенки кисты соответствует вторичному типу или ложным кистам, поскольку отсутствует эпителиальная выстилка. Заключение. В случаях ВКЗП лапароскопическое иссечение являются безопасным и эффективным методом с меньшей послеоперационной болью и более коротким периодом восстановления по сравнению с открытыми вмешательствами.
РАЗНОЕ
Учебник авторов К.Ш. Ганцева, Ш.Р. Кзыргалина, Ф.В. Моисеенко, Р.С. Ямиданова под редакцией профессора Ш.Х. Ганцева «Онкология 2.0» является продолжением многолетнего издательского труда авторов, который происходит на протяжении более 20 лет и посвящен раскрытию механизмов современной модели канцерогенеза, так как именно данное понимание является одним из условий успешного диагностического поиска и лечебного процесса в онкологии. Особую актуальность данный факт приобретает в современных условиях, когда онкология становится все более наукоемкой дисциплиной и для успешного ее освоения необходим синтез знаний из различных областей науки. Учебник успешно реализовал задачу академического изложения сложного материала в доступной форме, объединив обширные знания по молекулярной биологии, генетике, клинической и экспериментальной онкологии, анатомии, лимфологии, а также уникальные собственные научные разработки.
ISSN 2307-0501 (Online)