ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Введение. Бедренный доступ для эндоваскулярных операций сохраняет свою актуальность, однако его выполнение связано с риском возникновения фатальных и нефатальных осложнений. Современные технологии аппаратного гемостаза, достигаемого с помощью устройства «Angioseal» («Terumo Corporation», Япония), предоставляют возможность снижения числа фатальных и нефатальных осложнений.
Цель исследования. Провести многоцентровую оценку эффективности и безопасности аппаратного закрытия пункционного отверстия с применением устройств «Angioseal» в различных условиях и клинических ситуациях.
Материалы и методы. Проведен многоцентровой ретроспективный анализ 1088 случаев использования устройства «Angioseal» для осуществления «первичного» и «осложненного» аппаратного гемостаза после бедренного доступа в период с 2018 по 2020 год. Средний возраст пациентов составил 62,3 ± 11,6 года. Мужчин было 845 (78,0 %), женщин — 243 (22,0 %). В исследовании приняли участие пять центров, осуществляющих плановую и экстренную рентгенэндоваскулярную помощь.
Результаты. Применение устройства «Angioseal» показывает высокую эффективность метода — 97,0 % успеха «первичного» аппаратного гемостаза (1055 случаев из 1088 успешных процедур гемостаза) в условиях различных клинических ситуаций. В структуре осложнений (3,0 %) — тромбоз артерий на стороне доступа составил 5 случаев из 33 наблюдений; остальные варианты осложнений были связаны с геморрагическими событиями (8 случаев) или отказом/повреждением устройства, наблюдаемым в 20 случаях.
Обсуждение. По данным проведенного исследования мы заключили, что случаи «осложненного» аппаратного гемостаза были сопряжены с техническими трудностями применения устройства и требовали заблаговременного планирования. Ключевыми моментами успешного применения устройства «Angioseal» можно считать прямолинейность прохождения якоря устройства по доставляющей трубке через мягкие ткани в просвет сосуда и контроль расположения якоря в сосуде.
Заключение. Конструктивные особенности и методика аппаратного гемостаза с применением устройства «Angioseal» в 97 % случаев позволяют эффективно и безопасно осуществлять первичное закрытие пункционного артериального доступа.
Введение. В конце 2019 года в Китайской Народной Республике выявлена новая коронавирусная инфекция. 11 марта 2020 г. Всемирная организация здравоохранения объявила о начале пандемии COVID19. В течение 2018 года выявлено 2068 пациенток со злокачественными новообразованиями вульвы, пик заболеваемости приходится на возраст 75–79 лет. Основной метод лечения пациенток с диагнозом рака вульвы (РВ) — хирургический. По мнению большинства авторов, хирургическое лечение — единственный метод, позволяющий достичь хороших отдаленных результатов. Одним из методов уменьшения объема хирургического лечения пациенток с данным диагнозом является селективная биопсия сторожевого лимфатического узла (СЛУ).
Цель исследования: применение методики определения СЛУ при РВ с целью снижения объемов оперативного лечения, хирургических осложнений и длительности госпитализации в условиях пандемии COVID19.
Материалы и методы. Представлен опыт хирургического лечения 19 пациенток со злокачественными новообразованиями вульвы. Все пациентки находились в зоне риска по осложненному течению COVID19 ввиду возраста и сопутствующей патологии. В 13 случаях произведена вульвэктомия с биопсией сторожевого лимфатического узла. Детекция СЛУ проводилась методом радиоизотопной лимфосцинтиграфии.
Результаты и обсуждение. Отмечено уменьшение сроков госпитализации в этой группе больных и отсутствие хирургических осложнений, характерных для лимфаденэктомий. Также немаловажным фактором является сокращение сроков нахождения пациенток в стационаре.
Заключение. Сокращение времени госпитализации в условиях пандемии COVID19 является актуальной задачей. Методика определения СЛУ у пациенток с инвазивным плоскоклеточным раком вульвы с T1A–T2 является эффективной, позволяющей сократить объем оперативного лечения. Вульвэктомия с определением СЛУ представляет собой операцию выбора в условиях жестких противоэпидемиологических мероприятий при пандемии COVID19.
Введение. Острые кровотечения, возникающие из паренхиматозных органов при ушибах мягких тканей твердыми тупыми предметами, разрезах колющережущими предметами и разрывах пулями и осколками, часто угрожают жизни пострадавших изза гипоксии на фоне геморрагического шока. Гипоксия и геморрагический шок развиваются изза непрерывного истечения крови из множества зияющих кровеносных сосудов, лишенных способности сужаться. Безопасный и эффективный метод хирургического органосохраняющего лечения паренхиматозных кровотечений окончательно не разработан.
Материалы и методы. Проведен обзор научной и патентной литературы по способам гемостаза при кровотечениях из паренхиматозных органов путем локальных хирургических воздействий, дополненных локальными охлаждениями и нагреваниями. Исследование проведено с использованием баз данных Espacenet, Google Patent, eLibrary, Google Scholar, Web of Science, Scopus и PubMed.
Результаты и обсуждение. Показано, что в конце ХХ века в России был предложен оригинальный способ остановки паренхиматозного кровотечения. Метод основан на поперечном безопасном сдавливании органа в области сосудистого ствола, обеспечивающем безопасную ишемию травмированной части органа, и локальном нагревании раневой поверхности, обеспечивающем активацию свертывания крови. Сдавливание органа осуществляется с помощью хирургического инструмента, который обычно используется для мягкого сдавливания желудка и кишки. Механическое сдавливание органа осуществляется с силой, обеспечивающей полное пережатие его кровеносных сосудов и остановку вытекания крови из зияющих кровеносных сосудов раны. Локальная гипертермия раневой поверхности осуществляется с помощью прикладывания к ней твердого стерильного предмета с ровной гладкой и скользкой поверхностью при температуре +42…+45 °С. Ишемия и нагревание кровоточащей части паренхиматозного органа прекращаются через 5–15 минут. Критерием адекватности метода является полный гемостаз.
Заключение. Показано, что для достижения максимально быстрого кровоостанавливающего эффекта во всех случаях паренхиматозных кровотечений нет альтернативы немедленному прекращению кровоснабжения раневой поверхности, дополненному ее нагреванием до +42…+45 °С вплоть до наступления окончательного гемостаза. Для профилактики развития послеоперационных спаек в брюшной полости предложено завершать хирургическую операцию орошением всей поверхности брюшины раствором 50 % глицерина при рН 7,4 и температуре +37…+42 °С.
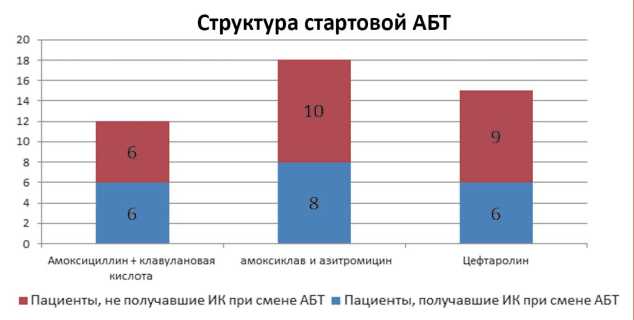
Введение.Одним из новых и недостаточно изученных направлений в современной пульмонологии является ингаляционное введение антибактериальных препаратов (АБП). К возможным преимуществам данного метода использования АБП относятся: доставка препарата непосредственно в очаг инфекции, достижение высокой концентрации антибиотика в трахеобронхиальном секрете и уменьшение риска развития системной токсичности. К наиболее частым АБП, которые вводятся ингаляционным путем, относятся аминогликозиды и полимиксин Е (колистин).
Цель работы: сравнительный анализ групп пациентов с тяжелой внебольничной пневмонией, вызванной Klebsiella pneumoniae, получавших и не получавших ингаляционный колистин.
Материалы и методы. Дизайн — ретроспективное многоцентровое контролируемое нерандомизированное исследование. В разработку включены 45 пациентов. 20 из них получали колистин, 25 — нет. Конечная точка — выживаемость. Для анализа полученных результатов использовалась программа Statistica 6.0.
Результаты и обсуждение. Основные клинические и лабораторные характеристики сравниваемых групп пациентов достоверно не отличались. Также не было отмечено различий при балльной оценке по шкалам тяжести состояния и исходов. Однако были получены статистически значимые отличия в сроках длительности ИВЛ (р = 0,04) и разрешения пневмонии (р = 0,044).
Заключение. Добавление ингаляционного полимиксина в схему терапии тяжелой внебольничной пневмонии, вызванной Kl. pneumoniae, достоверно снижает длительность ИВЛ и сроки разрешения пневмонии у пациентов пожилого и старческого возраста, но не влияет на выживаемость.
Введение. К сочетанным клапанным поражениям относятся поражения более чем одного клапана, что, в свою очередь, может затруднить правильную оценку степени тяжести состояния каждого клапана. Целью исследования стала оценка непосредственных результатов трансаортального протезирования митрального клапана (ТАПМК) при двухклапанном протезировании.
Материал и методы. На ретроспективное исследование были отобраны 19 пациентов, которым было выполнено ТАПМК при двухклапанном протезировании. Средний возраст больных составил 58,0 ± 8,6 года. Мужчин было 10. Сахарный диабет в анамнезе диагностирован у 3 пациентов, фибрилляция предсердий зарегистрирована у 14, ишемическая болезнь сердца — у 2, хроническая обструктивная болезнь легких — у 2, инсульт в анамнезе — у 1 пациента, хроническая сердечная недостаточность III–IV ФК по NYHA — у 19 больных. Инфекционный эндокардит в качестве этиологии порока обнаружен у 4 больных. Двое больных ранее оперированы на сердце. Эхокардиографические параметры: средняя фракция выброса левого желудочка составила 55,0 ± 7,3 %, среднее давление в легочной артерии — 47,0 ± 13,7 мм рт. ст., медиана диаметра фиброзного кольца аортального клапана — 23 (21–25) мм.
Результаты и обсуждение. В 12 случаях были имплантированы механические протезы. Медиана времени операции составила 160 (150–185) мин, среднее время ишемии миокарда (ИМ) — 67,0 ± 9,7 мин, время искусственного кровообращения (ИК) — 87,0 ± 12,5 мин. Рестернотомия по поводу кровотечения выполнялась двум больным, медиана послеоперационной кровопотери составила 300 (212–587) мл. Делирий в раннем послеоперационном периоде развился у 4, острая почечная недостаточность, потребовавшая гемодиализа, отмечалась у 1 больного. Инсульт, периоперационное повреждение миокарда и нарушение проводимости, потребовавшее имплантации электрокардиостимулятора, не отмечены в послеоперационном периоде. Медиана времени искусственной вентиляции легких (ИВЛ) составила 9,5 (6–15) часа, ИВЛ ≥24 часов — у 2. В раннем послеоперационном периоде умер один пациент.
Заключение. ТАПМК при двухклапанном протезировании — безопасная методика с коротким временем ИК, ИМ и длительности операции, которая может быть рекомендована к применению у пациентов с широким фиброзным кольцом АК.
КЛИНИЧЕСКИЙ СЛУЧАЙ
Введение. Одним из основных показателей качества лечения и профилактики эхинококкоза в отдаленном послеоперационном периоде является его рецидив, диапазон частоты которого широкий и в разных лечебных учреждениях составляет от 3 до 54 %. Одним из перспективных направлений в поиске этиопатогенетических факторов развития рецидивного эхинококкоза печени является исследование генетических особенностей заболевания, знание которых позволит прогнозировать возможное повторное развитие эхинококковых кист, а также подбирать индивидуальное лечение пациентов.
Материалы и методы. На базе Башкирского государственного медицинского университета (Россия, г. Уфа) проведен анализ клинического случая по оценке эффективности таргетной химиопрофилактики рецидивного эхинококкоза печени у пациента с генотипом CYP1A2F1*A/A (АА) с фенотипом — UM «быстрого» метаболайзера альбендазола сульфоксида в альбендазола сульфон.
Результаты и обсуждение. Наш клинический случай подтверждает целесообразность персонализированного подхода к химиопрофилактике рецидивного эхинококкоза альбендазолом в зависимости от результатов генетического анализа. Генетический анализ позволяет предположить, что обнаружение в крови пациента генотипа «быстрого» метаболайзера приведет к ускоренному разрушению альбендазола, принимаемого пациентом, и тем самым к снижению антипаразитарной эффективности лекарства по сравнению с фенотипом нормального метаболайзера, что будет способствовать рецидиву заболевания.
Заключение. Результаты успешной вторичной профилактики рецидива эхинококкоза подтверждают эффективность персонализированного подхода к химиопрофилактике рецидивного эхинококкоза альбендазолом в зависимости от результатов генетического анализа.
Введение. Кистозная гипоплазия легкого — порок развития, при котором терминальные отделы бронхиального дерева на уровне субсегментарных бронхов или бронхиол представляют собой расширения кистообразной формы различных размеров. Она составляет 60–80 % всех пороков развития.
Материалы и методы. На примере клинического случая представлены особенности клинической картины, диагностической роли лучевых методов исследования и выбор хирургической тактики диагностики и лечения кистозной гипоплазии легкого. Пациентка К., 57 лет, поступила в ГБУЗ «Республиканский клинический противотуберкулезный диспансер» (РКПТД) с диагнозом: фиброателектаз нижней доли правого легкого на фоне сахарного диабета II типа, ст. субкомпенсации, где была проконсультирована фтизиатром, торакальным хирургом и направлена на оперативное лечение.
Результаты и обсуждение. Тщательно собранный анамнез и данные лучевой диагностики в подавляющем большинстве случаев позволяют уверенно диагностировать врожденную природу кистозных изменений в легких. Выбор тактики лечения у таких пациентов проводят индивидуально, однако предпочтение отдают хирургическому. Только детальное и внимательное исследование патоморфологической ткани легкого, полученного во время хирургического лечения, очень часто дает возможность выставить верный диагноз.
Заключение. В диагностике данного заболевания решающая роль отводится современным инструментальным методам, и прежде всего мультиспиральной компьютерной томографии. Представляются важными и интересными публикации подобных наблюдений, обобщение которых поможет изучить причины возникновения заболевания.
Введение. Каждое чрескожное коронарное вмешательство (ЧКВ) потенциально может привести к грозным осложнениям, которые могут возникать в ходе операции. Рутинные манипуляции катетером, различными проводниками, системой доставки и стентом могут повредить стенку сосуда, вследствие чего незамедлительно развивается такое осложнение, как экстравазация. По данным интервенционных кардиологов, разрывы происходят в 0,19–0,93 % случаев ЧКВ. Эндоваскулярный хирург, столкнувшийся с данным осложнением во время операции, должен незамедлительно проанализировать ситуацию и принять решение о дальнейших действиях, чтобы устранить разрыв коронарной артерии.
Материалы и методы. В данной статье приведен клинический пример осложнения при ЧКВ — экстравазация IIICS типа при рутинном стентировании передней межжелудочковой артерии. С учетом и анализом всех факторов было принято решение имплантировать стентграфт в зоне перфорации.
Результаты и обсуждение. При выполнении чрескожного коронарного вмешательства необходимо быть готовым к любым осложнениям, исключением не являются и рутинные интервенции. Такое осложнение, как экстравазация, является прогнозируемым. Эндоваскулярный хирург должен обладать достаточным опытом для принятия решения и определения тактики дальнейших действий. Результат после имплантации стент графта является удовлетворительным.
Заключение. При возникновении осложнений во время ЧКВ в виде экстравазации IIICS типа методом выбора может стать имплантация стентграфта.
ОБЗОР ЛИТЕРАТУРЫ
больных SARS. В связи с вероятной ролью ретроэлементов в патогенезе COVID19 в качестве перспективных направлений лечения COVID19 могут быть предложены ингибиторы обратной транскриптазы LINE1 и таргетная терапия с использованием микроРНК.
ISSN 2307-0501 (Online)